
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
Психология и педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Рефераты по сексологии
Рефераты по информатике программированию
Краткое содержание произведений
Реферат: Витамины В12 и В15
Реферат: Витамины В12 и В15
Содержание
|
Введение Краткий исторический очерк Номенклатура корриноидов Химия витамина В12
Кислотный гидролиз витамина B12
Механизм действия
Некоторые В12-зависимые ферменты
Витамин В15
Клиника
Заключение Список использованной литературы |
3 4 4 6 7 7 8 8 9 9 10 11 11 12 12 13 14 15 16 16 16 17 20 21 23 23 24 24 25 25 25 26 27 27 28 29 29 29 31 31 32 33 34 |
Введение
Lascante ogni speranza voi ch’entrate!
Dante
Витамины (от лат. Vita – жизнь) - группа органических соединений разнообразной химической природы, необходимых для питания человека, животных и других организмов в ничтожных количествах по сравнению с основными питательными веществами (белками, жирами, углеводами и солями), но имеющих огромное значение для нормального обмена веществ и жизнедеятельности.
Первоисточником витаминов служат главным образом растения. Человек и животные получают витамины непосредственно с растительной пищей или косвенно – через продукты животного происхождения. Важная роль в образовании витаминов принадлежит также микроорганизмам. Например, микрофлора, обитающая в пищеварительном тракте жвачных животных, обеспечивает их витаминами группы В. Витамины образуют в организме большое количество разнообразных производных (например, эфирные, амидные, нуклеотидные и др.), которые, как правило, соединяются со специфическими белками, выступая в роли коферментов. Наряду с ассимиляцией, в организме постоянно осуществляется диссимиляция витаминов, причем продукты их распада, а иногда и малоизмененные молекулы витаминов выводятся наружу. Недостаточность снабжения организма витаминами ведет к его ослаблению, резкий недостаток витаминов – к нарушению обмена веществ и заболеваниям – авитаминозам, которые могут закончится гибелью организма. Авитаминозы могут возникать не только от недостаточного поступления витаминов с пищей, но и вследствие нарушения процессов их усвоения и использования организмом.
Основоположник учения о витаминах русский врач Н. И. Лунин установил (1880), что при кормлении белых мышей только искусственным молоком, состоящим из казеина, жира, лактозы и солей, животные погибают. Следовательно, в натуральном молоке содержатся другие вещества, незаменимые для питания. В 1912 году польский врач К. Функ предложил само название «Витамины», обобщил накопленные к тому времени экспериментальные и клинические данные и пришел к выводу, что такие заболевания, как рахит, цинга, пеллагра, бери-бери, - болезни витаминной недостаточности. С этого времени наука о витаминах (витаминология) начала интенсивно развиваться, что объясняется значением витаминов не только для борьбы со многими заболеваниями, но и для познания сущности ряда жизненных явлений. Метод обнаружения витаминов, примененный Луниным (содержание животных на специальной диете – вызывание экспериментальных авитаминозов), был положен в основу исследований.
Оба витамина, которым посвящен этот реферат, впервые были обнаружены в экстрактах печени высших животных. Действие обоих из них связано с переносом метильной группы от одной молекулы к другой, причем пангамовая кислота может являться донором метильной группы, а витамин В12 – промежуточным переносчиком. Однако если относительно принадлежности цианкобаламина к витаминам споров не возникает, то причисление к ним пангамовой кислоты оспаривается большинством ученых. В «Энциклопедическом Химическом Словаре», например, утверждается, что факт принадлежности пангамовой кислоты к витаминам не доказан, Березовский в своей книге «Химия Витаминов» приводит статью о пангамовой кислоте в заключающей книгу рубрике «Некоторые биологически активные вещества». Вообще сведения о витамине В15, доступные мне, оказались весьма скудны и в основном затрагивают вопросы его клинического применения в ущерб химическим свойствам.
Краткий исторический очерк
Витамин В12, пожалуй, самый сложный из всех витаминов, впервые заявил о себе научному миру, когда в 1926-м году американские врачи Джордж Мино и Уильям Мэрфи обнаружили, что включение в состав питания больших количеств полусырой печени оказывает лечебное воздействие при злокачественной анемии. Однако попытки выделения антианемического фактора к успеху не привели. Лишь в конце 40-ых годов Мэри Шорб обнаружила вид бактерий, рост которых зависел от этого фактора, благодаря чему у ученых появилась возможность оценивать содержание витамина в данном субстрате по скорости роста колонии. В 1948 г. Э. Лестер Смит (Англия), а также Эдвард Рикес и Карл Фолкерс (США) получили витамин В12 в кристаллическом виде.
Однако потребовалось еще десять лет для того, чтобы методом рентгеноструктурного анализа определить его структуру, которая оказалась чрезвычайно сложной. За расшифровку структуры витамина В12 (1955 г.) Дороти Ходжкин была присуждена нобелевская премия.
Витамин В15 (пангамовая кислота) был впервые обнаружен в 1950-м году Томиямой в экстракте печени быка. Название пангамовой кислоты происходит от латинских корней «пан» - всюду и «гами» - семя, так как позже она была обнаружена в составе семян огромного количества растений.
Номенклатура корриноидов
Ц
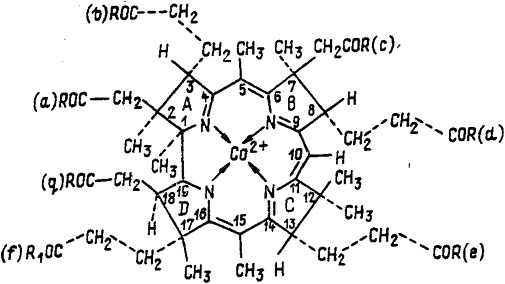
Рисунок 1. Структура корриноидов.
R1=OH – кобириновая кислота; R-NH2; R1=OH – кобировая кислота; R-OH; R1-остаток 1-амино-2-пропанола – кобиновая кислота; R=NH2; R1-остаток 1-амино-2-пропанола – кобинамид; R=OH; R1-остаток D-рибофуранозил-З-фосфата – кобамовая кислота; R-NH2: R1=остаток D-рибофуранозил-З-фосфата – кобамид
ианкобаламин относится к классу корриноидов - производных коррина, структура которого родственна порфирину. Однако, наряду с близостью их структур, имеются два важных химических различия между этими макроциклами. В то время как порфирин содержит систему из 12 сопряженных двойных связей, коррин состоит из частично восстановленных пиррольных (пирролиновых) гетероциклов. Корриновое кольцо содержит 6 двойных связей, входящих в состав линейной сопряженной системы, включающей 12 из 15 атомов, составляющих внутренний контур макроцикла. Корриновое кольцо сужено по сравнению с порфириновым. Если в порфирине каждая пара пиррольных колец отделена метиновыми мостиками, то в коррине кольца А и D соединены непосредственно связью между α-положениями. Поэтому внутренний контур корринового макроцикла содержит на один атом углерода меньше, чем порфириновый.
В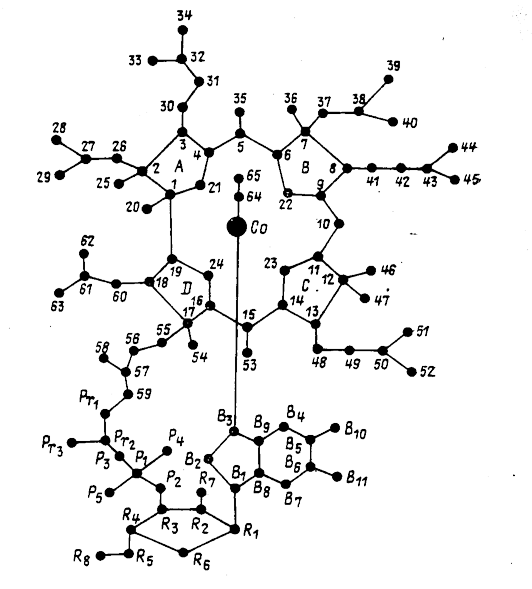
Рисунок 2. Нумерация атомов в молекуле цианкобаламина.
соответствии с номенклатурой корриноидов, утвержденной в 1975 г. Международной комиссией по биохимической номенклатуре, органический экваториальный лиганд, состоящий из четырех восстановленных пиррольных колец с атомом кобальта в центре, назван коррином, а соединения его содержащие - корриноидами. Гептакарбоновая кислота, изображенная на рис. 1, названа кобириновой кислотой. Карбоксильные группы обозначены буквами а-g, как показано на этом рисунке. a,b,c,d,e,g-гексаамид кобириновой кислоты назван кобировой кислотой. Кобиновая кислота является амидом кобириновой кислоты с D-1-амминопропанолом-2 в положении f; его гексаамид назван кобинамидом. Кобамовая кислота является фосфодиэфирным производным кобиновой кислоты, в котором гидроксил 2 положения аминопропанола замещен остатком α-D-рибофуранозил-З-фосфата; его гексаамид назван кобамидом. Кобамиды, которые имеют 5,6-диметилбензимидазольный лиганд, связанный гликозидной связью через N1 с С1 рибофуранозы, называются кобаламинами. Корриноиды, имеющие в α-аксиальном положении вместо 5,6-дииметилбензимидазола другие основания, также называются кобамидами.
Химия витамина В12
В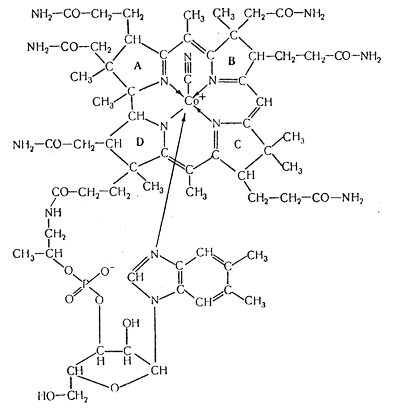
Рисунок 3. Структура цианкобаламина.
итамин B12 кристаллизуется в виде темно-красных игл или призм; цвет варьирует в зависимости от величины кристаллов. Кристаллы темнеют при 210-220°, но не плавятся при температуре ниже 3000Ц. Первыми установленными константами были показатели преломления, а именно α = 1,616, β = 1,652, γ = 1,664. Кристаллографические измерения показывают, что кристаллы относятся к орторомбической системе и имеют призматическую форму. При кристаллизации из водного раствора и из смеси воды с ацетоном они содержат значительное, но изменчивое количество непрочно связанной кристаллизационной воды. Ее можно удалить нагреванием при пониженном давлении, причем кристаллы не теряют своей формы. После этого обезвоженный материал может снова поглощать влагу из атмосферного воздуха в количестве 10-12%; это и есть тот продукт, который обычно выпускается под названием витамина B12 и зарегистрирован в фармакопеях Англии и США. Витамин B12 довольно хорошо растворим в воде (около 1,2% при комнатной температуре), а также в низших спиртах, в низших алифатических кислотах и в фенолах, но нерастворим во многих других органических жидкостях. Он практически не растворяется в пиридине и других третичных аминах, но растворим в некоторых жидких или расплавленных амидах, например в ацетамиде и диметилформамиде. Витамин является левовращающим веществом, но интенсивная, окраска затрудняет измерение оптического вращения. Витамин B12 обладает диамагнитными свойствами, что указывает на трехвалентное состояние кобальта.Обычно витамин выделяют из микробной массы или животных тканей, используя растворы, содержащие цианид-ионы, играющие роль шестого лиганда кобальта. Однако сам цианкобаламин метаболически не активен. В состав ферментов входит соединение, в котором цианогруппа замещена остатком 5-дезоксиаденозина или метильным радикалом.
Строение
Признанная формула витамина B12 – C63H88O14N14PCo. Молекулу можно подразделить на две основные части, известные как "планарная группа" и "нуклеотид"; вторая часть лежит в плоскости, почти перпендикулярной к плоскости первой части, которая обладает очень большим, хотя и неполным, сходством с порфиринами Центральный атом кобальта соединен с четырьмя восстановленными пиррольными кольцами, образующими макрокольцо. Три из четырех соединений между кольцами образованы мезоуглеродным атомом (углеродным мостиком), характерным для порфиринов. Однако в четвертом месте соединения существует прямая связь между двумя α-углеродными атомами колец D и А. Макрокольцо содержит 6 сопряженных двойных связей, образующих единую сопряженную систему.
У 13 из 19 углеродных атомов, составляющих макрокольцо, водород полностью замещен метильными группами или длинными боковыми цепями – либо ацетамидными, либо пропионамидными радикалами
В отличие от нуклеотидов нуклеиновых кислот так называемый нуклеотид витамина B12 не содержит пурина или пиримидина. Вместо них основанием служит 5,6-диметилбензиминазол. Сахар представлен рибозой, но с α-гликозндпой связью, опять-таки в отличие от β-связи в нуклеиновых кислотах. Рибоза фосфорилирована при 3-м атоме углерода. Фосфат образует эфирную группу с 1-амино-2-пропиловым спиртом, который, кроме того, соединен амидной связью с цепью пропионовой кислоты при кольце D. Наконец, атом кобальта несет CN-группу (в цианкобаламине) и соединен координационной связью с одним из атомов азота в бензиминазоле, образуя, таким образом, второй мостик между двумя частями молекулы. Полагали, что третий гидроксил фосфатной группы тоже этерифицирован, пока не стало ясно, что неустойчивость триэфиров фосфорной кислоты исключает такую структуру. Витамин B12 является по существу внутренней солью; отрицательный заряд на атоме фосфора нейтрализован положительным зарядом на координационном комплексе кобальта.
Кобаламины
Первые химические данные о витамине B12 содержались в одновременных сообщениях из лаборатории Глаксо и Мерка, в которых указывалось на присутствие в его молекуле кобальта и фосфора. Самые ранние английские публикации касались второго красного фактора, появляющегося на хроматограммах наряду с витамином B12; Этот фактор был получен в кристаллическом виде Пирсом и его Сотрудниками в лаборатории Ледерле и был назван витамином B12b. Тем временем исследователи из лабораторий Мерка описали витамин В12а как вещество, образующееся при обработке витамина В12 водородом в присутствии платинового катализатора. Позже он оказался идентичным витамину В12b. В лабораториях Глаксо было описано еще одно родственное соединение – витамин B12c. В 1950 г. отношения между этими "витаминами B12" выяснились в результате почти одновременных сообщений из лабораторий "Органон" (Голландия) и Мерка, в которых было показано, что витамин B12 содержит группу цианида, соединенную координационной связью с кобальтом. Группу цианида можно было удалить фотолизом или путем восстановления в определенных условиях с выходом витамина B12a, который, как предполагали, содержит на месте цианида гидроксильную группу. При обработке водным раствором цианида витамин B12a быстро превращается в тот пурпурный дицианидный комплекс, который возникает из самого витамина B12. После подкисления вторая группа цианида теряется и остается витамин B12. Для всей молекулы B12, исключая группу цианида, был предложен термин "Кобаламин", так что витамин B12 стал называться цианкобаламином, а витамин B12a оксикобаламином. Эта терминология получила широкое признание.
Путем обработки витамина B12a различными кислотами удалось получить ряд других аналогов. К ним относится витамин B12c, содержащий группу азотистой кислоты; он был назван нитриткобаламином, или нитрокобаламином. По-видимому, витамин B12a обычно существует не в форме оксикобаламина, а в форме аквокобаламина, молекула которого содержит нейтральную молекулу воды, что сообщает всему координационному комплексу основные свойства; это согласуется с данными о том, что соединение титруется как основание. Можно получить другие основные кобаламины, содержащие вместо воды молекулу аммиака или некоторых аминов. Кроме этих основных и нейтральных соединений, существует еще класс кислых кобаламинов. Из них наиболее известно пурпурное вещество, образующееся при добавлении избытка цианида, к витамину B12. Оно содержит 2 молекулы цианида, соединенные координационными связями с кобальтом. Бивен и сотр. получили довольно убедительные спектроскопические данные о наличии координационной связи между свободным атомом азота в бензиминазоле и кобальтом. Избыток цианида разрывает ее, по-видимому, потому, что ион цианида образует с металлом более прочную координационную связь. Дицианосоединение, однако, устойчиво только в щелочном растворе. Дицианкобаламин легко замещает цианогруппу на ОН-, NO2-, SO3-, Cl-, Br-, SCN- и пр. Все производные в присутствии цианид-ионов превращаются в цианкобаламин.
Устойчивость и взаимопревращения различных классов Кобаламинов изучали с помощью изотопов и другими методами. Все эти вещества без исключения превращаются в витамин B12 под действием цианида. Неудивительно поэтому, что все они обнаруживают биологическую активность в отношении микроорганизмов, а также животных и больных пернициозной анемией, хотя некоторые из них менее активны, чем цианкобаламин.
До сих пор мы рассматривали витамин В12 как нейтральное вещество, хотя в действительности это чрезвычайно слабое основание. Это обнаружилось еще в ранних исследованиях при титровании в растворах уксусной кислоты.
Кислотный гидролиз витамина B12
При обработке витамина B12 неорганическими кислотами в различных условиях получено много продуктов расщепления. Одним из первых был идентифицирован аммиак, образующийся при гидролизе амидных групп. Химическое изучение концентратов антипернициозного фактора привело к предположению, что он представляет собой вещество полипептидной природы. Однако при исследовании кислотных гидролизатов обычным методом хроматографии на бумаге в чистых образцах кристаллического витамина не нашли никаких признаков наличия α-аминокислот. Тем не менее, группа исследователей из Британской палаты медицинских препаратов обнаружила на хроматограмме пятно, дающее нингидриновую реакцию*; эта реакция была обусловлена не аминокислотой, а пропаноламином.
При взаимодействии с концентрированной HCl при 65оС происходит отщепление нуклеотида и образование кобинамида (фактора В – см. ниже), затем происходит отщепление и образование кобировой кислоты (фактора V1a).
Нуклеотид
При кислотном гидролизе витамина B12 в жестких условиях образуется 5,6-диметилбензиминазол. Было показано, что полностью нуклеотид соответствует названию 1-α-D-рибофуранозид-5,6-диметилбензиминазол. Сомнительным оставалось только то, в каком положении - 2 или 3 - фосфорилирована рибоза. Окончательно этот вопрос был решен лишь с помощью рентгеноструктурного анализа.
Продукты мягкого кислотного гидролиза
В первом приближении, мягкий гидролиз разбавленной хлороводородной кислотой приводит к частичному дезаминированию, последовательному образованию моно-, ди-, три-, тетра-, пента-, гекса-, гептакарбоновых кислот с сохранением нуклеотида.
Продолжительная обработка витамина B12 холодной разведенной соляной кислотой приводила к медленной потере микробиологической активности, при этом интенсивность красной окраски не изменялась. Было обнаружено, что с увеличением длительности гидролиза возникает все более сложная смесь продуктов. Среди них одно-, двух-, трех- и четырехосновные кислоты, образующиеся при последовательном удалении аммиака из амидных групп. При добавлении азотистой кислоты в этих условиях образовывались также небольшие количества пяти- и шестиосновных кислот, обладающих красной окраской. Монокарбоновые кислоты можно разделить на три. Дикарбоновые кислоты также разделяются на три изомера; трикарбоновые кислоты фракционировать не удавалось. Этого и следовало ожидать при случайном гидролизе трех лабильных амидных групп. Относительные количества получаемых изомеров показывали, что одна из этих групп значительно лабильнее остальных. Три остальные амидные связи гидролизовались только при обработке кислотой в более жестких условиях или при каталитическом воздействии азотистой кислоты. Когда в результате рентгеноструктурного анализа строение витамина было выяснено, появилась возможность истолковать эти наблюдения. Три лабильные амидные группы, очевидно, принадлежат трем цепям пропионамида, а три стабильные группы - ацетамидным цепям.
Это описание продуктов кислотного гидролиза упрощено, так как, за исключением случаев самого мягкого гидролиза, при электрофорезе выявлялась еще одна группа кислот. Эти кислоты образуются в результате отщепления не только ряда молекул аммиака, но также и нуклеотида.
В водном растворе при мягком кислотном гидролизе (а также фотолитически или при каталитическом гидрировании) цианкобаламин, через промежуточную стадию В12r (см. Восстановление витамина В12) с последующим окислением кислородом воздуха переходит в оксикобаламин.
Фактор В
Исследователи из лаборатории Глаксо нашли, что молекулу витамина можно аккуратно разделить на две части кратковременным нагреванием с концентрированной соляной кислотой или, еще лучше, с хлорной кислотой. При тщательно контролируемых условиях (например, 5 мин при 65°) амидные группы почти не подвергались гидролизу и главными продуктами были, нуклеотид и неизмененная остальная часть молекулы. Последний продукт сохранял микробиологическую активность и оказался идентичным природному фактору, выделенному из содержимого рубца жвачных. В присутствии цианида растворы этого вещества имели пурпурную окраску даже при слабо кислой реакции среды. Спектр поглощения был очень сходен со спектром дицианкобаламина, так что в этом состоянии вещество почти наверное содержало два остатка цианида, соединенных координационной связью с кобальтом. Однако в то время как дицианкобаламин имел кислотные свойства, новое соединение было нейтральным. Причина такого различия состояла в отщеплении кислого нуклеотидного остатка. Это наблюдение по существу явилось главным основанием для представления о витамине B12 как внутренней соли.
Ряд кислот, образующихся при гидролизе амидных групп в факторе В, обладал той же относительной стабильностью в их дициано-конфигурации.
Были получены указания на то, что существует 7-я карбоксильная группа, связанная не с аммиаком, а через амин с нуклеотидом. Это подтверждало более раннее предположение о том, что аминопропиловый спирт служит мостиком между двумя частями молекулы, будучи соединенным амидной связью с одной из цепей пропионовой кислоты в планарной группе и эфирной связью - с фосфорной кислотой. В кислых растворах (с рН примерно менее 3) фактор В теряет обе группы цианида и ведет себя как основание. Соответствующие кислоты ведут себя сходным образом, так как карбоксильные группы не подвергаются заметной ионизации. Поэтому все вещества, не содержащие нуклеотида, можно отделить от веществ, еще сохранивших его.
Щелочной гидролиз
Жесткий щелочной гидролиз приводит к отщеплению 5,6-диметилбензимидазола и образованию дилактампента- и монолактамгексакарбоновых кислот.
П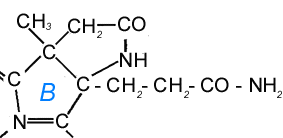
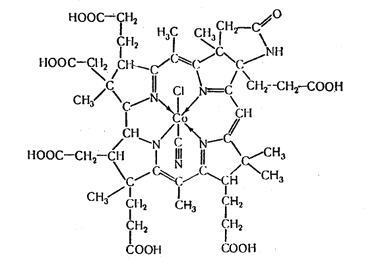
Рисунок 4. Рисунок 4. Дегидровитамин В12 (Строение кольца В корринового макроцикла и прилегающих к нему структур)
Рисунок 5. Гексакарбоновая кислота, образующаяся при щелочном гидролизе.
ри обработке витамина B12 перекисью водорода и разведенной щелочью на холоду и получаются микробиологически активные кислые продукты красного цвета. Реакция состоит в гидролизе, катализируемом перекисью водорода. Однако полученные кристаллические продукты, по-видимому, представляли собой смеси моно- и дикарбоновых кислот, образовавшихся в результате мягкого гидролиза, с неизмененным витамином B12, который обусловливал их биологическую активность. Под действием холодной разведенной щелочи, по-видимому, образуются те же продукты, что и при мягком кислотном гидролизе. Однако в присутствии горячей щелочи реакция идет по-иному. Если нагревать витамин B12 в растворе NaOH в отсутствие кислорода, то окраска становится коричневой, а затем приобретает зеленоватый оттенок, это может указывать на уменьшение валентности атома кобальта, сопровождающееся окислением какой-то другой части молекулы. При доступе воздуха цвет снова становится красным. Кратковременное кипячение со щелочью при доступе воздуха дает в качестве главного продукта нейтральное кристаллизующееся красное вещество. Оно почти неотличимо от витамина B12 по физическим свойствам, но не обладает микробиологической активностью. Структура этого соединения была выяснена главным образом путем рентгеноструктурного анализа кристаллов. Продукт, по-видимому, содержит лактамное кольцо, имеющее 2 общих атома с кольцом В и образующееся из ацетамидной цепи; остальная часть молекулы такая же, что и в самом витамине. Добавление тиогликолата натрия или цианида натрия к раствору витамина в основном защищает его от воздействия щелочи и кислорода. Полагают, что реакция протекает при участии свободных радикалов. Производное, содержащее лактам, было названо дегидровитамином B12. Лактамное кольцо чрезвычайно устойчиво и при дальнейшем воздействии щелочи сохраняется. При гидролизе последовательно отщепляются остающиеся амидные группы и нуклеотид. Таким образом, получаются два ряда кислот – с нуклеотидом и без нуклеотида, - но все они отличаются от соответствующих продуктов кислотного гидролиза. Конечным продуктом щелочного гидролиза является гексакарбоновая кислота, а не гептакарбоновая, как при кислотном гидролизе. Это связано с участием одной из потенциальных кислотных групп в построении лактамного кольца. Основное значение этого кристаллического продукта распада состоит в использовании его для рентгеноструктурного анализа.Продукты окисления
Исследование
гидролиза дало
ценные сведения
о том, что можно
было бы назвать
периферией
молекулы. Гораздо
труднее оказалось
изучить химическими
методами структуру
части молекулы,
непосредственно
окружающей
атом кобальта.
Кембриджская
группа показала,
что среди продуктов
окисления
витамина B12
нельзя обнаружить
амида м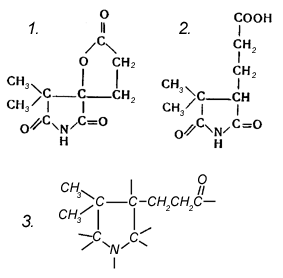
Рисунок 6. Продукты окисления.
алеиновой кислоты, так что вряд ли можно было относить витамин к истинным порфиринам. Но эти исследователи выделили в довольно большом количестве оксамовую кислоту. Единственные азотсодержащие продукты расщепления "ядра" молекулы выделили в 1955 г. Фолкерс и сотр. Контролируемое окисление хроматом натрия в уксусной кислоте привело к образованию двух продуктов, изображенных на рисунке 6 (1 и 2). Полагали, что они образуются из группировки, имеющей пирролидиновую, пирролиновую или пирролениновую структуру (рис. 6, 3). Это были первые химические данные, указывающие на присутствие пирролоподобной структуры в молекуле, если не считать более ранних данных по пиролизу, позволявших предполагать такую структуру. Несколько позже был выделен и соответствующий продукт, содержащий амидную группу (амид кислоты, представленной на рис. 6, 2). Это явилось прямым химическим подтверждением местоположения по крайней мере, одной из амидных групп.При окислении цианкобаламина Н2О2 в среде с рН меньше семи наблюдается выход продуктов, обладающих антагонистическим биологическим действием для lactobacillus leichmannii, в отличие от ростового для Euglena gracilis. При окислении перманганатом калия отщепляется синильная кислота, а также образуются уксусная кислота, щавелевая кислота и ее амид, бутандиовая кислота, 2-метилбутандиовая и 2,2-диметилпропандиовая кислоты.
Восстановление витамина B12
При каталитическом гидрировании на платиновом катализаторе цианкобаламин присоединяет пять атомов водорода и отщепляет метиламин, кобальт переходит в двухвалентное состояние с образованием т. н. В12r. При длительном восстановлении и при использовании более сильных восстановителей, таких как ацетат хрома при рН 9,5 или борогидрид натрия получают так называемый В12s, содержащий одновалентный кобальт.
Восстановление внесло разочаровывающе малый вклад в наши знания о строении витамина, и даже теперь детальная структура продуктов восстановления еще достаточно не выяснена. Обработка водородом в качестве катализатора или некоторыми другими восстановительными агентами вызывает переход окраски в коричневую и, наконец, в серо-зеленую. Эти изменения, за исключением потери цианида, обратимы при контакте с кислородом воздуха, причем образуется витамин B12а. Вопрос об изменениях валентности кобальта, происходящих при восстановлении. Работа Бивена и Джонсона, появившаяся после опубликования предположительной структуры витамина, пролила некоторый свет на не решенный еще вопрос о том, содержит он 5 или 6 сопряженных двойных связей.
Обратимое восстановление легко продемонстрировать, добавляя к щелочному раствору витамина B12 тиогликолевую кислоту. Красная окраска медленно переходит в оранжево-бурую; после встряхивания раствора в присутствии воздуха она тотчас же вновь становится красной. По мере использования кислорода снова медленно появляется цвет восстановленного витамина B12. Эти изменения окраски можно повторно вызывать почти до бесконечности: окончательный результат состоит в том, что витамин катализирует окисление тиогликолевой кислоты (по-видимому, до дисульфида) кислородом воздуха.
Реакция с галогенами
Хлор обесцвечивает раствор цианкобаламина, другие галогены – нет. Продуктом хлорирования является фиолетовое кристаллическое вещество.
Энергичное хлорирование витамина B12 давало продукт, содержащий 30% хлора, природа его не была охарактеризована точнее. Петров и сотр. описали ряд продуктов, образующихся при обработке витамина хлором или хлорамином Т, которые можно было разделить методом хроматографии. Эти вещества имели пурпурный цвет, переходящий при избытке цианида в голубой, и содержали 2 атома хлора в молекуле.
Воздействие одной молекулы хлорамина Т или брома дает в качестве главного продукта нейтральное кристаллизующееся вещество красного цвета. По физическим свойствам оно было очень сходно с витамином B12, но не обладало микробиологической активностью. Электрофорез и инфракрасная спектроскопия доказали, что это был лактон; полагают, что его строение идентично строению лактама показанного на рис. 5, только вместо NH следует поставить О. Образование лактона, по-видимому, связано с промежуточным образованием иона карбония в активированном β-положении кольца В.
Йод действует на витамин B12 только в щелочных растворах, и при этом образуются как лактам, так и лактон, относительные количества которых зависят от концентрации щелочи и йода.
Дальнейшая обработка хлорамином Т или бромом вела к образованию пурпурных веществ, которые становились голубыми при избытке цианида и содержали в молекуле соответственно хлор или бром. Эти продукты не были полностью охарактеризованы, но сходное вещество, возникавшее при действии хлорамина Т на лактам (дегидровитамин B12), было изучено в Кембридже, и оказалось, что оно содержит только один атом хлора. Полагают, что хлор замещал водород при мезоуглеродном атоме между кольцами В и С. Эта работа в сочетании с другими данными помогла установить, что в молекуле витамина имеется 6 сопряженных двойных связей, а не 5, как предполагалось вначале.
Метилирование
При действии избытка СН3-HgJ на JCbl в спиртовом растворе при температуре 65оС в течение трех часов можно получить метилкобаламин с выходом около 50%. Вообще реакциями корриноидов с сильными нуклеофилами получают соответствующие органокорриноиды.
М![]()
ежду
диметилсульфатом
и самим витамином
B12 никакой
реакции не
происходит,
так как атом
азота участвует
в координационной
связи с кобальтом.
Эта связь должна
быть сначала
разорвана путем
превращения
витамина B12
в дицианкобаламин;
даже и после
этого реакция
зависит от
значения рН.
Образующийся
при этом четвертичный
азот обусловливает
возникновение
добавочной
основной группы
в молекуле
дицианида,
которая в результате
этого, обладает
нейтральной
реакцией (а не
кислой, как
молекула
дицианкобаламина);
эта структура
устойчива в
кислых растворах,
так как метилирование
препятствует
образованию
координационной
связи между
N3 и Со. Эта реакция
была использована
для изучения
более сложных
свойств аналога
витамина B12
– фактора III,
который может
быть метилирован
или в любом из
двух положений
или в обоих
одновременно.
Рентгеноструктурный анализ
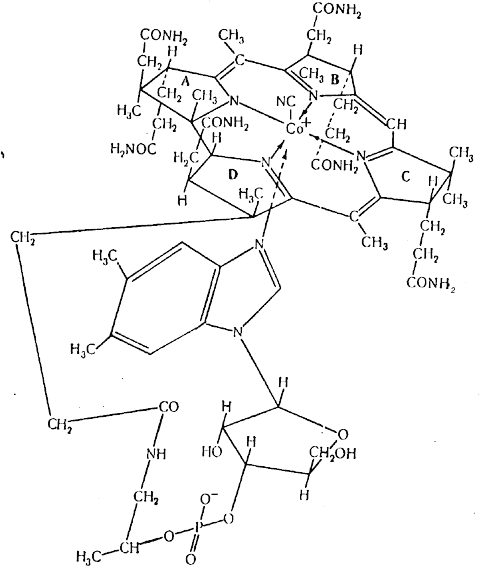
И
Рисунок 7. Пространственная конфигурация молекулы витамина В12.
зучение витамина B12 методом рентгеноструктурного анализа начала Дороти Ходжкин в Оксфорде в 1948 г., как только были получены первые кристаллы. Независимо подобную же работу проводил Уайт в Принстоне; позже обе группы исследователей объединили свои силы. Трудоемкие вычисления на основе результатов измерения отражении рентгеновских лучей позволили составить карты электронной плотности в трех измерениях. Постепенно, в несколько последовательных этапов, по мере того как определялось положение все большего числа атомов в структуре, расчеты уточнялись. Вся программа работы с витамином B12 и теми его аналогами, которые были получены, потребовала примерно около 10 млн. вычислений. Для этого на последних этапах пришлось использовать электронные счетные машины. Никогда еще рентгеноструктурный анализ не применялся для изучения структуры столь сложной молекулы, и полный успех этой программы изучения явился замечательным достижением, несколько смутившим химиков-органиков и, кажется, удивившим даже самих специалистов по рентгеноструктурному анализу. Как заметила Дороти Ходжкин, "возможность записать химическую структуру главным образом на основании чисто кристаллографических данных о размещении атомов в пространстве – и притом для такой устрашающе сложной молекулы - это для всякого кристаллографа нечто похожее на мечту". Огромное преимущество этого метода состояло в том, что в отличие от химических методов он "работает" от центра к периферии. Иными словами, относительно тяжелый атом кобальта с наибольшей точностью указывал положение ближайших к нему атомов, а именно атомов макрокольца. Когда работа приближалась к завершению, оказалось, что единственными атомами, положение которых оставалось несколько сомнительным, были те, для которых оно было выяснено Фолкерсом и его сотрудниками в результате изучения продуктов окисления витамина. Вычисления, относившиеся к самому витамину B12, были на время отложены, когда исследователи смогли получить кристаллическую гексакарбоновую кислоту. Это более простое соединение неожиданно легко поддавалось рентгеноструктурному анализу, в связи с чем и были достигнуты большие успехи. К счастью, основные структурные особенности этого вещества и самого витамина оказались идентичными, так что исследования этих веществ взаимно дополняли друг друга. Однако они в обоих случаях независимо привели к весьма редкой структуре макрокольца. Макрокольцо содержит 4 восстановленных пиррольных кольца с прямой α-α-связьюю между кольцами А и D. Дальнейшие уточнения в расчётах сделались возможными в результате изучения двух кобаламинов, содержащих относительно тяжелые атомы, а именно производных тиоцианата и селеноцианата; позже для этой же цели был использован аналог витамина B12, содержавший два атома хлора на месте метильных групп у бензиминазола. Наконец, выяснилась природа боковых цепей, и можно было почти с полной уверенностью написать всю структурную формулу. Все оставшиеся сомнения были, по-видимому, разрешены дальнейшими вычислениями, позволившими даже установить, что в макрокольце 6 двойных связей.
Устойчивость
В литературе накопилось много данных об устойчивости витамина B12 к действию как реактивов, так и лекарственных препаратов; многие из этих данных можно теперь истолковать, исходя из строения и реактивности различных частей молекулы витамина. Кристаллический цианкобаламин в твердом состоянии устойчив даже при действии температуры 100° в течение нескольких часов. По Березовскому, при нагревании кристаллического цианкобаламина при 100° происходит медленное разложение. В водных растворах он наиболее устойчив при рН от 4 до 6 (по Березовскому до 7); в этих пределах рН растворы можно стерилизовать автоклавированием при 120° с потерей лишь нескольких процентов активности. При pH 9 происходит быстрое разложение (примерно 90% в сутки).
Аквокобаламин менее устойчив, особенно в щелочном растворе, но оба вещества инактивируются примерно на 90% в течение 1 часа при 100° при рН 8. Нагревание в сильно щелочном растворе использовали для количественного разрушения витамина B12 с целью контроля при некоторых методах микробиологического определения активности. Однако в неочищенных препаратах некоторые восстанавливающие вещества могут оказывать защитное действие. Нейтральные или слегка кислые растворы витамина B12 при комнатной температуре в темноте сохраняются годами, только в очень сильно разведенных растворах идет медленный гидролиз с образованием небольших количеств фактора В. В сильно кислых и, особенно в щелочных растворах при комнатной температуре происходит медленный гидролиз до карбоновых кислот. На свету цианид медленно отщепляется и образуется оксикобаламин, но при выдерживании раствора в темноте происходит обратный процесс. Длительное воздействие солнечного света ведет к необратимому разрушению. Характер действия восстановителей не всегда можно предсказать с уверенностью. Утверждают, что тиоловые соединения в низких концентрациях защищают витамин от разрушения, и их даже используют иногда с этой целью при микробиологических определениях, однако в больших количествах они сами могут вызвать разрушение витамина. Сульфит также рекомендовали применять для защиты Кобаламинов, особенно оксикобаламина. Аскорбиновая кислота действует не так, как другие, восстановители. Она довольно быстро разрушает витамин B12b, но почти не действует на витамин B12. Данное наблюдение использовали при анализе смесей этих двух веществ, но такой метод пригоден лишь для сравнительно чистых растворов. В печеночных экстрактах содержится защитный фактор, которым оказалось железо; другие металлы, например медь, катализируют реакцию. В сухих лекарственных препаратах витамин B12 устойчив при растирании в порошок с хлористым натрием или с маннитом. Растворы можно стабилизировать фенолом, подвергнутым двойной перегонке, хотя примеси, содержащиеся иногда в феноле, могут вызывать разрушение витамина. Совместное присутствие тиамина (витамина B1) и никотинамида (или никотиновой кислоты) ведет к медленному разрушению витамина B12 в растворе. Железо защищает витамин В12 от взаимодействия с никотиновой кислотой.
Механизм действия
Недостаток в пище витамина B12 приводит к макроцитарной мегалобластической анемии. Нарушается работа нервной системы, наблюдается резкое снижение кислотности желудочного сока. Впрочем, авитаминоз В12 может развиться даже при полноценном питании, т. к. для процесса всасывания витамина в тонкой кишке обязательно наличие в желудочном соке особого белка – гастромукопротеина (фактор Касла). В полном соответствии с буквальным переводом своего латинского названия, этот белок выделяется стенками желудка, теми же клетками, которые выделяют кислоту. Фактор Касла специфически связывает витамин В12. Точная роль этого фактора не выяснена. Полагают, что в составе комплекса с гастромукопротеином витамин всасывается в тонком кишечнике и поступает в кровь портальной системы в комплексе с транскобаламинами I и II, при этом фактор Касла гидролизуется.
Когда биохимики привыкли к мысли, что витамин В12 не просто специфический антипернициозный фактор, а один из витаминов группы В, они стали предполагать, что он подобно другим водорастворимым витаминам окажется кофактором по крайней мере в одной ферментной системе. Но вопреки ожиданию функции, приписываемые витамину B12 различными исследователями, оказались столь многочисленными и разнообразными, что трудно было представить себе, как все они могли быть связаны с такой ролью кофактора. Поэтому стали искать его основную функцию. Например, казалось вероятным, что он каким-то образом ответствен за поддержание сульфгидрильных соединений в восстановленном реактивном состоянии; он мог бы, скажем, "активировать" различные SH-ферменты, препятствуя их окислению в неактивные S-S-формы. Или если он связан с синтезом белка, он был бы необходим для синтеза белковой части (апофермента) ряда ферментов.
Позднейшие исследования, особенно с применением изотопов, поставили под сомнение некоторые из приписываемых витамину В12 функций и выдвинули на первый план другие. Однако ряд новейших результатов еще не подтвержден.
Отношение к сульфгидрильным ферментам
Влияние концентрата витамина B12 на восстановление некоторых S-S-соединений в SH-форму изучал в o1950 г. Дубнов на ферментных системах in vitro. Он высказал предположение, что восстановлением гомоцистина в гомоцистеин, легко присоединяющий метильную группу, можно, было бы объяснить действие витамина B12 на синтез метионина. Поддержание глутатиона в восстановленномм состоянии могло бы играть роль в активации SH-ферментов. Эти гипотезы были подкреплены последующими наблюдениями. При рецидивах пернициозной анемии, а также у крыс, получающих рацион с недостатком витамина В12 концентрация сульфгидрильных соединений (главным образ6м глутатиона) в крови ниже нормальной, и в обоих случаях она поднимается до нормы или после введения витамина. Быстрота этой реакции позволяет думать, что это непосредственный результат действия витамина. Однако Жаффе вовсе не обнаружил подобного действия у мышей.
Согласно Лингу и Чоу и другим авторам, при авитаминозе В12 нарушено использование углеводов. Это могло бы быть связано с низкой концентрацией глутатиона двояким образом. Сульфгидрильные группы некоторых гликолитических ферментов могли бы окисляться до неактивной S-S-формы: в частности, глутатион является простетической группой одного ключевого фермента – глицеральдегид-3-фосфатдегидрогеназы. Позднее Дубнов подверг дальнейшей проверке свою гипотезу реактивации SH-ферментов, использовав покоящиеся клетки мутанта Е. coli, нуждающегося в витамине B12. Он нашел, что активность ряда таких ферментов вначале была так же высока, как и в клетках "дикого" штамма, но снижалась по мере старения культур и могла быть вновь повышена добавлением витамина B12 или глутатиона, причем гораздо эффективнее было добавление их обоих.
Обмен жиров и каротина
Благотворное действие витамина В12 на обмен жиров у животных аналогичным образом приписывали поддержанию кофермента А в активном восстановленном состоянии. У крысят, получающих рацион с недостатком витамина B12, организм не способен синтезировать жиры, а у взрослых крыс нарушается использование жиров пищи так что животные становятся тучными в результате избыточного накопления жира. Полагают, что этот эффект лишь частично объясняется, действием витамина B12 на синтез метионина, в результате которого, в свою очередь, увеличивается количество липотропных веществ – холина и бетаина. Установлено, что витамин B12 повышает всасывание каротина или превращение его в витамин А у крыс (на что указывает повышенное накопление последнего в печени); хотя и не влияет на накопление готового витамина А. Механизм этого действия еще неясен.
Участие витамина B12 в биохимических
восстановительных процессах
Утверждали, что витамин В12 помимо действия на сульфгидрильные соединения поддерживает в восстановленном состоянии другие важные вещества. Так, Уилл и сотр. установили, что в плазме больных пернициозной анемией содержание аскорбиновой кислоты понижено; кроме того, при инъекции таким больным аскорбиновой кислоты она быстро окисляется в дегидроаскорбиновую. После лечения витамином B12 эти явления исчезают, а инъекции аскорбиновой кислоты ведут к повышению ее концентрации в плазме. Чоу и сотр. нашли, что в печени крыс с недостаточностью витамина В12 общее содержание дифосфопиридиннуклеотида повышено, но количество его восстановленной формы (ДПН-Н) понижено. Ненормально высокое отношение ДПН/ДПН-Н снижалось вдвое после введения витамина B12.
Было высказано предположение, что витамин B12 способен играть роль восстановителя, когда его трехвалентный кобальт восстановлен до двухвалентного состояния. Однако нужны сильные восстановители, чтобы вызвать эту реакцию, которая в присутствии атмосферного кислорода идет в обратном направлении. Предположение о том, что соединение с белком могло бы сдвинуть окислительно-восстановительный потенциал в область физиологических величин, не вполне убедительно, так как способность связывать белок после восстановления, возможно, утрачивается.
Биосинтез метионина и серина
Метилкобаламин участвует в реакциях синтеза метионина в качестве кофактора. Заключительным этапом синтеза метионина у бактерий, грибов, высших растений и животных состоит в переносе метильной группы от СН3-ТГФК к сульфгидрильной группе гомоцистеина.
Существует
два типа ферментов,
осуществляющих
синтез метионина
– первый, независимый
от кобаламинов,
может использовать
в качестве
донора метильной
группы только
триглутаматную
форму СН3-ТГФК.
Второй тип
ферментов,
зависимый от
кобаламиновых
кофакторов,
может использовать
как моно-, так
и триглутаматную
форму СН3-ТГФК.
Для активации
ферментов
второго типа,
кроме того,
требуется
S-аденозилметионин
(S-AdoMet).
Последний
необходим для
первоначального
метилирования
кобаламина.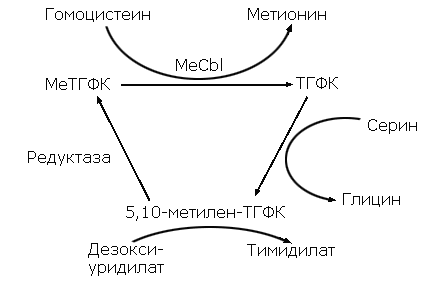
Схема 1. Биосинтез метионина.
Мутант Е. coli, используемый для определения витамина В12, способен так же хорошо расти и при добавлении к минимальной питательной среде метионина, только для оптимального роста требуется примерно в 10000 раз больше метионина, чем витамина. Очевидный вывод, что в клетках этого организма витамин действует как катализатор синтеза метионина, был подтвержден экспериментально. Однако для любого другого микроорганизма, нуждающегося в витамине B12, этот витамин не может быть заменен метионином, так что он, очевидно, осуществляет у этих организмов какую-то дополнительную функцию.
|
Скармливаемый предшественник |
Радиоактивность метильного углерода метионина, μ с/г-атом |
Повышение биосинтеза метионина, % |
|
|
В присутствии вит. В12 |
В отсутствие вит. В12 |
||
|
При неограниченном потреблении пищи |
|||
|
α-14С-Глицин (2%) β-14С-Серин (0,7%) 14С-Формиат натрия (0,1%) |
156 81,5 33,8 |
95,5 47,4 20,0 |
63 72 69 |
|
При ограниченном потреблении пищи |
|||
| 14С-Формиат натрия (0,1%) | 32,0 |
28,6 |
12 |
Таблица 1. Влияние витамина В12 на биосинтез метионина.
Р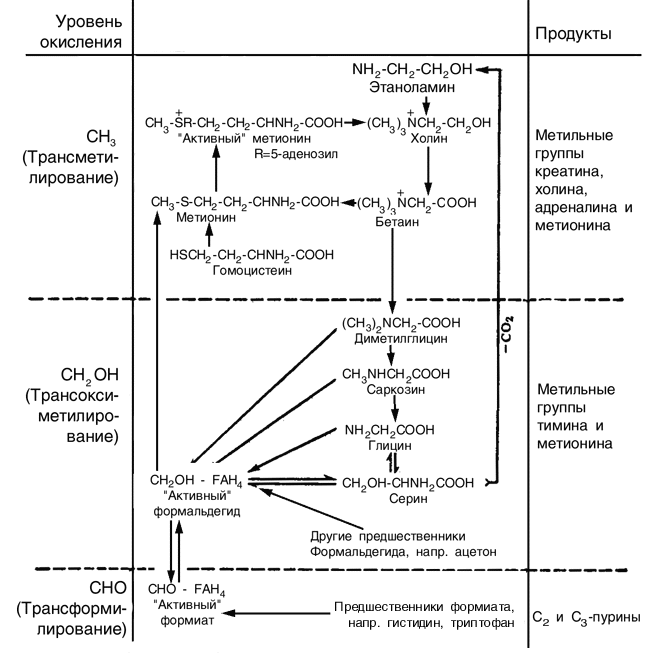
Схема 2. Этапы переноса радикала с одним углеродным атомом.
анние эксперименты с изучением роста цыплят и крыс также показали, что витамин B12 снижает потребность в метионине, особенно при введении гомоцистеина. Сначала это было истолковано как действие витамина на трансметилирование, т. е. на передачу лабильной метильной группы от холина или бетаина к гомоцистеину с образованием метионина. Точно так же витамин B12 может, по крайней мере частично, заменять холин для цыплят, крыс и поросят-сосунков. Ряд исследований (некоторые из них с использованием 14С) показал, что витамин B12 не оказывает никакого влияния на трансметилирование, но участвует в прямом синтезе лабильной метильной группы из более окисленных предшественников – таких, как формиат, α-углерод глицина или β-углерод серина. Трудности истолкования результатов, получаемых на интактных животных, хорошо иллюстрирует таблица 1.П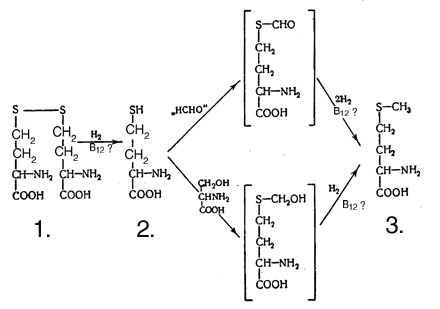 ри
авитаминозе
В12 сильно
ухудшается
аппетит и наблюдаемые
результаты
часто могут
быть обусловлены
просто пониженным
потреблением
пищи по сравнению
с контрольными
животными. Эту
неясность можно
устранить,
ограничив
потребление
пищи контрольными
животными до
уровня, х
ри
авитаминозе
В12 сильно
ухудшается
аппетит и наблюдаемые
результаты
часто могут
быть обусловлены
просто пониженным
потреблением
пищи по сравнению
с контрольными
животными. Эту
неясность можно
устранить,
ограничив
потребление
пищи контрольными
животными до
уровня, х
Схема 3. Этапы превращения гомоцистина в метионин.
1 – Гомоцистин; 2 – Гомоцистеин; 3 - Метионин
арактерного для авитаминозных животных (метод "парного кормления"). Подтверждение данных для поросят и цыплят в опытах с 14С-формиатом и 14С-серином получили Джонсон и сотр. Однако при использовании меченого формальдегида результат оказался неожиданным: интенсивность включения метки в метильные группы метионина и холина у цыплят с недостаточностью витамина B12 оказалась значительно повышенной. Есть основательные данные в пользу того, что новообразованные метильные группы появляются в метионине, но потом в результате трансметилирования они могут оказаться в холине или креатине. Эти выводы никто не оспаривал, но некоторые исследования позволяли предположить, что, кроме того, при недостаточности витамина B12 у крыс активность трансметилазы в печени понижена.Значение витамина B12 в переносе групп с одним атомом углерода почти неразделимо переплетается с функциями фолиевой кислоты (точнее, производных тетрагидрофолевой кислоты). Эти процессы переноса, которые могут происходить на трех различных уровнях окисления, схематически представлены на схеме 2, показаны также связанные с ними реакции окисления и восстановления. Некоторые из этих процессов переноса происходят в несколько этапов (не показанных на схеме 2) это, безусловно, относится к превращению гомоцистина в метионин, и почти нет сомнений, что для реакции в целом необходимы оба витамина. Возможная последовательность этапов показана на схеме 3.
Как уже говорилось, витамину B12 приписывали участие в восстановлении гомоцистина до гомоцистеина – акцептора метильной группы. Однако последующие опыты с мечеными аминокислотами показали, что витамин, возможно, не нужен для этого восстановления. Какое-то производное фолиевой кислоты, несомненно, участвует в самом переносе радикала с одним углеродным атомом. Тогда единственная функция, остающаяся для витамина B12, состоит в восстановлении этой группы в метильную группу метионина – если только витамин не действует лишь косвенным образом, способствуя, например, синтезу ферментов. Во всяком случае, синтез метионина не может быть единственной биохимической функцией витамина В12 у высших животных, так они гибнут от его недостаточности даже при большом количестве метионина и холина в пище.
Сопоставление данных, приводимых в пользу и против участия витамина B12 во взаимопревращениях глицина и серина, приводило скорее к выводу об отсутствии влияния витамина, но работа Вора и сотр. вскрыла новую сторону проблемы. Эти авторы не обнаружили снижения общего синтеза серина из α-14С-гли-цина в срезах печени индейки, но наблюдали значительное уменьшение включения 14С в положении 3. Они объясняют это тем, что витамин B12 действует на этапе отщепления от глицина радикала с одним углеродным атомом, перенос которого осуществляет тетрагидрофолевая кислота. Если это подтвердится, то, по-видимому, такой же механизм мог бы действовать в синтезе метильной группы метионина de novo.
Также по механизму трансметилирования у некоторых бактерий происходит синтез уксусной кислоты и метана:
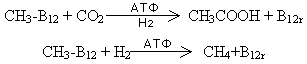
Синтез нуклеиновых кислот
С самого начала работ в данной области считали почти несомненным, что витамин B12 стимулирует синтез дезоксирибонуклеиновой и, вероятно, рибонуклеиновой кислот. Молочнокислые бактерии, используемые для определения витамина B12, почти так же хорошо растут при замене его большими количествами тимидина или других дезоксирибонуклеозидов; проще всего это можно объяснить тем, что витамин B12 участвует в каком-то этапе синтеза ДНК. Выяснилось, что действие витамина связано с синтезом дезоксирибозного компонента ДНК. Некоторые ученые полагают, что у некоторых бактерий витамин B12 стимулирует синтез не только ДНК, но и РНК.
Однако другие микроорганизмы, нуждающиеся в витамине B12, не способны расти на дезоксирибозидах, и нет данных о том, что у этих видов витамин контролирует синтез ДНК. У мутанта Е. coli равномерно меченный уридин превращался в тимин не только в присутствии витамина B12, но и в присутствии метионина; кроме того, у него не наблюдалось превращения меченой рибозы в дезоксирибозид. Тем не менее была тенденция переносить выводы из опытов с молочнокислыми бактериями также и на высших животных, включая человека. Этому способствовал факт энергичной регенерации эритроцитов и роста эпителия языка после лечения рецидивов пернициозной анемии цианкобаламином. Здесь действительно должен происходить быстрый синтез нуклеиновых кислот, но возможно, что этот процесс подавляется при недостаточности витамина, так как для пролиферации клеток необходимы и другие компоненты. Кроме того, активность костного мозга при пернициозной анемии отнюдь не подавлена; в самом деле, кругооборот компонентов гема примерно втрое превышает нормальный уровень, но большая часть этой активности бесполезна для образования новых эритроцитов. Ряд исследователей отмечает пониженное содержание ДНК, РНК или обеих нуклеиновых кислот в организме животных при авитаминозе В12; истолкование таких результатов усложняется тем, что авитаминозные животные потребляют меньше пищи. О`Делл и Бруммер использовали радиоактивный фосфат и нашли, что лишение как витамина B12, так и пищи вообще действительно оказывает сходное влияние на синтез нуклеиновых кислот. Глейзер и сотр. установили, что в мегалобластическом костном мозге человека отношение урацил/тимин и соответственно отношение РНК/ДНК значительно выше нормального. После лечения витамином B12 или фолиевой кислотой обе величины быстро уменьшались до нормы. Предложенное объяснение состояло в том, что витамин B12 катализирует синтез компонента ДНК – тимина; метилирование урацила с образованием тимина формально аналогично метилированию гомоцистеина с образованием метионина – реакции, которую, как известно, стимулирует витамин B12. Однако в этом исследовании, к сожалению, определяли относительные, а не абсолютные количества, между тем более ранняя работа Дэвидсона и указывает на возможность иного объяснения результатов. Эти авторы нашли, что в мегалобластическом костном мозге содержание ДНК и особенно РНК ненормально повышено в расчете как на 1 г, так и на 1 клетку; после лечения количество обеих кислот уменьшалось (правда, количество РНК - быстрее), что и должно было вести к изменению отношений, найденному Глейзером и его сотрудниками.
|
Введенный предшественник |
Радиоактивность выделенных нуклеиновых кислот, имп/мин/мг |
|||
|
Полноценный рацион |
Рацион, лишенный вит. В12 |
|||
| РНК | ДНК | РНК | ДНК | |
|
У свиней |
||||
|
14С-Формиат 14С-Серин 14С-Глюкоза |
360 266 255 |
316 232 260 |
318 266 230 |
356 226 235 |
|
У кур |
||||
|
14С-Формиат 14С-Формальдегид 14С-Глицин 14С-Серин 14С-Н3-Метионин |
680 590 460 308 440 |
605 482 328 325 360 |
625 470 388 330 409 |
582 505 305 330 320 |
Таблица 2. Влияние витамина В12 на синтез нуклеиновых кислот.
Позже в опытах с изотопами стали искать более прямых данных. Исследовали, например, влияние витамина B12 на включение радиоактивного фосфора в нуклеиновые кислоты. Витамин B12 стимулировал включение его во фракцию ДНК кишечника и селезенки, но не печени и в то же время не влиял на радиоактивность РНК. Джонсон и сотр. использовали еще более прямой подход к проблеме: они изучали включение 14С из различных предшественников (формиата, формальдегида, глицина, серина и глюкозы) в нуклеиновые кислоты печени свиней, кур и крыс; у крыс они определяли также превращение некоторых из этих предшественников в аллантоин. Ни в одном случае нельзя было обнаружить сколько-нибудь значительного влияния витамина B12 на радиоактивность ДНК, РНК или аллантоина. Если эти данные будут подтверждены, то трудно будет признавать связь между витамином В12 и синтезом нуклеиновых кислот у высших животных. Мистри и Джонсон в опытах на курах действительно установили, что витамин B12 повышает синтез мочевой кислоты из формиата, метильной группы метионина или β-углеродного атома серина, но не из формальдегида или глицина; однако они трактуют это не как результат прямого действия на биосинтез пуринов, а как возможное влияние на какую-то окислительную реакцию в обмене соединений с одним углеродным атомом.
Белковый обмен
Очевидно, что благодаря своему влиянию на синтез метионина витамин B12 оказывает какое-то действие на белковый обмен. Например, можно ожидать, что цианкобаламин будет улучшать использование белка из рационов, в которых этой аминокислоты недостаточно. Таким образом объясняли некоторые из отмеченных выше благотворных эффектов витамина. Значительную прибавку в весе тела, даже если она связана с увеличением количества не только жира (как часто бывает), но и белка, обычно можно объяснить просто повышенным потреблением пищи животными, получающими витамин B12. Не было обнаружено никакого влияния витамина B12 на баланс азота и эффективность использования белков у крыс. Различные исследования, однако, указывали на более прямую роль этого витамина в синтезе белка. Так, было установлено, что у крыс с гипертиреозом (гиперфункцией щитовидной железы) витамин B12 способствует удержанию азота. У кур при недостаточности витамина B12 концентрация аминокислот в крови повышена, а белков в плазме – понижена; у человека также показано обратное отношение между концентрациями аминокислот и витамина B12 в крови, что объясняется стимулирующим действием витамина на синтез белков. Сообщается об избыточном выведении с мочой аминокислот, особенно лизина (но также и таурина) при обострении пернициозной анемии и дегенерации спинного мозга. Нарушение нормального обмена тирозина и триптофана могло бы вести к избыточному выделению фенольных веществ, тоже отмеченному при пернициозной анемии, и, возможно, к образованию токсичных веществ, вызывающих гемолиз, которым иногда сопровождается это заболевание; все эти обменные нарушения быстро исчезают после введения витамина B12. Было отмечено, что при дегенерации спинного мозга, часто сопровождающей пернициозную анемию, поражаются некоторые крупные аксоны, нормальное состояние которых поддерживается быстрым обновлением белка. Поэтому исследователи предположили, что витамин B12, специфически излечивающий это состояние, косвенным образом контролирует синтез белка; полагая, что прямое действие витамина направлено на синтез нуклеиновых кислот, они связали свое предположение с гипотезой о том, что РНК служит "шаблоном" для синтеза белка; их данные было бы логичнее истолковать в пользу прямого действия витамина B12 на синтез белков.
Изучалось влияние витамина B12 на включение меченого серина или меченой глюкозы в белки печени и в некоторые отдельные аминокислоты у свиней и крыс. Во всех опытах полученные величины были заметно ниже у животных с авитаминозом. Исследователи приводят соображения в пользу того, что это не было следствием одного лишь пониженного потребления пищи. Данные наблюдения были дополнены исследованиями, проведенными in vitro на препаратах микросом из печени и селезенки нормальных крыс и крыс с авитаминозом. Как показано, между этими группами животных обнаружились большие различия во включении меченых аминокислот; кроме того, при добавлении витамина B12 к препаратам микросом, полученных от животных с авитаминозом, включение аминокислот заметно возрастало.
Ученые пошли дальше и показали, что в надосадочной жидкости после центрифугирования микросом печени находится содержащий витамин B12 «рН5-фермент», катализирующий включение меченых аминокислот в белок. Интересно было бы выяснить, не обладает ли ферментативной активностью комплекс витамина B12 с пептидом, выделенный ранее из печени. Позднее было показано, что «рН5-фермент» содержит большую часть витамина В12, первоначально находившегося в микросомах печени. Этот фермент подвергли дальнейшему фракционированию; он, по-видимому, катализировал как активацию аминокислот аденозинтрифосфатом, так и их последующее включение в белковую фракцию микросом. Кроме того, оба процесса подавлялись антагонистами витамина В12 содержащими остаток анилида вместо одной из амидных групп. Исследователи высказали гипотезу, что витамин В12-фермент действует как активатор-переносчик: он переносит аминокислоты (после активации их карбоксильных групп аденозинтрифосфатом) на "шаблон", возможно, путем транспептидирования, в котором участвуют 6 карбоксамидных групп молекулы витамина. Некоторые ученые приводят соображения, позволяющие предполагать, что некоторые из карбоксамидных групп являются биохимически активными частями молекулы. Другим исследователям пока не удалось подтвердить эти данные; они указывают также, что включение аминокислот в белок микросом не обязательно представляет собой нормальный синтез белка. Таким образом, эти результаты нельзя считать окончательным доказательством прямого действия цианкобаламина на белковый синтез. Однако это привлекательная гипотеза; контролем синтеза апоферментов можно было бы объяснить влияние витамина В12 на ряд, казалось бы, не связанных между собой ферментных систем. В пользу этого можно привести и другие данные; различные исследователи утверждали, что недостаточность витамина B12 у крыс ведет к уменьшению содержания в их печени некоторых ферментов, а именно трансметилазы, рибонуклеазы, цитохромоксидазы и различных дегидрогеназ. Другие авторы установили, что при отсутствии витамина B12 не происходит регенерации ткани печени после частичной гепатэктомии. Все эти данные говорят в пользу прямого или косвенного влияния витамина на синтез белка.
Другие возможные функции
Недостаток цианкобаламина в пище ведет к повышенному выделению тиоцианата; в связи с чем была выдвинута гипотеза, основанная на предполагаемой лабильности групп цианида и конкуренции за цианид между оксикобаламином и ферментом роданезой.
Тесная взаимосвязь между функциями фолиевой кислоты и цианкобаламина привела к предположению о том, что последний катализирует превращение фолиевой кислоты в "цитроворум-фактор" или какую-то другую активную форму; убедительных экспериментальных данных в пользу этого, по-видимому, нет.
Интересные взаимоотношения, видимо, существуют также между витамином B12 и пантотеновой кислотой. Некоторые исследователи утверждали, что в опытах с кормлением кур каждый из этих факторов снижал потребность в другом. Эванс и сотр. обнаружили уменьшение содержания пантотеновой кислоты в печени после введения витамина В12 курам с авитаминозом и предположили, что витамин мобилизует печеночные резервы пантотеновой кислоты. Другие исследователи подтвердили эту взаимосвязь и отметили повышенное содержание витамина B12 в организме крыс с недостаточностью пантотеновой кислоты. Гершоф и сотр. доказали наличие взаимосвязи между тироксином, магнием и витамином B12. Как магний, так и витамин B12 частично снимают ряд эффектов введения тироксина, потерю витамина B12 тканями, подавление роста, разобщение окисления и фосфорилирования, изменение белковых фракций сыворотки. Эти результаты еще ждут своего объяснения.
«Конца пути еще не видно, но есть основания надеяться, что скоро мы будем знать о механизме действия витамина B12 больше, чем мы знаем о действии некоторых других витаминов, открытых гораздо раньше»
Некоторые В12-зависимые ферменты
В12-коферменты многочисленны и различны. Они отличаются тем, что содержат два типа лигандов: метильную группу и 5`-дезоксиаденозин.
Превращение свободного витамина В12 в кофермент происходит в присутствии специфических ферментов и при участии в качестве кофакторов ФАД, восстановленного НАД, АТФ и глутатиона.
При образовании 5-дезоксикобаламинового кофермента АТФ подвергается необычному распаду с отщеплением трифосфатного остатка по аналогии с реакцией синтеза 5-аденозилметионина из метионина и АТФ.
Впервые В12-коферменты были выделены Г. Баркером с сотрудниками в 1958 г. из микробов.
Химические реакции с участием В12-коферментов подразделяют на две группы: реакции трансметилирования и изомеризации. В реакциях первой группы коферменты играют роль промежуточных переносчиков метильной группы. К таким реакциям относятся, например, синтезы метионина и ацетата. Гомоцистеин под воздействием метилкобаламина и тетрагидроилглутаматметилтрансферазы в присутствии восстановленного ФАД и N5-СН3-ТГФК *превращается в метионин. Метильная группа N5-СН3-ТГФК переносится вначале на активный центр фермента, затем на гомоцистеин. Ко второй группе реакций относится изомеризация L-метилмалонил-КоА в сукцинил-КоА.
Диолдегидратаза
Приведем вначале важнейшие данные, полученные за последние годы при исследовании диолдегидратазы, т. е. фермента, катализирующего превращение этандиола-1,2, и пропандиола-1,2, соответственно, в ацетальдегид и пропионовый альдегиды. Оказалось, что один и тот же фермент способен катализировать превращение и этандиола-1,2 и пропандиола-1,2 в соответствующие альдегиды. Примечательной особенностью этого фермента, как и всех остальных аденозилкобаламин-зависимых ферментов, явилось то, что окончание реакции сопровождается деструкцией и высвобождением кофермента из фермент-коферментного комплекса.
Диолдегидратаза представляет собой белок с мол. массой 250000 с единственным активным центром содержащим аденозилкобаламин. Хроматография позволяет разделить фермент на две субъединицы с разными молекулярными массами. Каждая из субъединиц неактивна, рекомбинация их приводит к восстановлению активности. Весьма важным и, по-видимому, общим свойством всех аденозилкобаламин-ферментов, является чувствительность диолдегидратазы к сульфгидрильным ингибиторам. Образование тройного ферментного комплекса (апофермент-АденозилКобаламин-пропандиол-1,2) полностью защищает фермент от действия ртутьсодержащих ингибиторов. Это позволяет утверждать, что HS-группа (или группы) фермента может иметь большое значение для проявления биокаталитической активности. Важно подчеркнуть, что защищающим действием, помимо аденозилкобаламина, обладают и другие Кобаламины (CN-Кобаламин, метилкобаламин), введение которых в ферментный комплекс вместо кофермента приводит к его инактивации. Тем не менее расщепление такого комплекса после обработки SH-соединением и последующая реконструкция с аденозилкобаламином вновь восстанавливает активность. Изучение химической модификации этого фермента выявило большое значение различных аминокислотных остатков в активном центре фермента. Так оказалось, что один остаток аргинина на моль фермента является необходимым для проявления каталитической активности диолдегидратазы. Наконец, недавно было продемонстрировано значение другой основной аминокислоты – лизина для проявления ферментативной активности. Остаток лизина, важный для обеспечения активной олигомерной структуры фермента и связывания аденозилкобаламина, локализован в низкомолекулярной субъединице. Остатки основных аминокислот обеспечивают ионное взаимодействие между субъединицами.
Глицеролдегидратаза
Другой фермент, катализирующий превращения вицинальных гликолей в альдегиды – глицеролдегидратаза или глицеролгидролиаза ответственен за изомеризацию глицерина в β-оксипропионовый альдегид и продуцируется как некоторыми штаммами Klebsiella р., так и Propionibactereciae. Кофакторами, необходимыми для проявления активности глицеролдегидратазы, являются аденозилкобаламин и К+. Очистка фермента из Кl. р. привела к выделению ферментного комплекса с мол. массой 188000, содержащего две субъединицы разного размера и 1 моль аденозилкобаламина на 1 моль фермента. Меньшая субъединица с мол. массой 22 000 в свою очередь распадается на два белка с мол. массой около 12 000. Самосборка субъединиц в ферментном комплексе промотируется субстратом – глицерином, аденозилкобаламином и ионом К+. Интересно, что ион Na+ ингибирует активность фермента и ни одна из субъединиц по отдельности не способна связывать аденозилкобаламин.
Аналогично диолдегидратазе, глицеролдегидратаза ингибируется сульфгидрильными ингибиторами, причем в опытах с обработкой субъединиц и последующей сборкой было показано, что меньшая субъединица после обработки еще сохраняет 25% от первоначальной активности, в то время как большая полностью ее теряет.
Этаноламин-аммиак-лиаза
Фермент, осуществляющий превращение этаноламина в ацетальдегид и аммиак – этаноламин-аммиак-лиаза – был описан в 1965 г., очищен и выделен в гомогенном состоянии в 1968 г.
Этот аденозилкобаламин-фермент интенсивно исследовался в работах Бэбиора и Ейбилиса. Итоги изучения фермента можно суммировать следующим образом: оказалось, что, в отличие от диолдегидратазы, единственным субстратом этаноламин-аммиак-лиазы является этаноламин. Позднее было выяснено, что L-2-аминопропанол также может превращаться в пропионовый альдегид и аммиак. Однако это превращение сопровождается необратимым расщеплением кофермента. При реакции NH2-гpyппa всегда перемещается от С2 к С1 (т. е. к атому, с которым связана ОН-группа). В опытах с меченым 18О Н2О было показано, что гидроксил при С1 всегда остается в продукте. Тем самым был исключен механизм образования ацетальдегида через промежуточный имин, гидролиз которого обязательно привел бы к включению метки в продукт. Наблюдаемый во всех аденозилкобаламин-зависимых реакциях перенос водорода С1→С2 был обнаружен и в этой реакции. Опыты с энантиомерами многократно меченого субстрата - 2-амино-[22H, 23Н]-этанола свидетельствовали о рацемизации продукта (ацетальдегида). Несмотря на то, что прямых доказательств перемещения NH2-группы от С2 к С1 не было получено, процесс превращения этаноламина в ацетальдегид и аммиак описывается по аналогии с другими реакциями.
Фермент представляет собой довольно большой белок с мол. массой 520000. В пятимолярном растворе гуанидин-НСl он диссоциирует – на субъединицы с мол. массой 50000. Показано, что фермент содержит два независимых активных центра. Подобно диолдегидратазе фермент активируется одновалентными катионами К+ и NH4+ и ингибируется сульфгидрильными ингибиторами.
Аденозилкобаламин-зависимые мутазы
Следующую группу Аденозилкобаламин-ферментов, составляют мутазы, катализирующие перегруппировки углеродного скелета и приводящие к обратимым превращениям субстратов с разветвленной цепью в соединения с прямой цепью. Среди этих ферментов хорошо изучены два – глутаматмутаза и метилмалонил-СоА-мутаза.
Глутаматмутаза
Фермент, катализирующий превращение L-глутамата в L-трео-β-метиласпартат, был выделен, из Clostridium tetanomorphum. Показано, что многочисленные фотосинтезирующие микроорганизмы также содержат глутаматмутазу. Фермент, кроме аденозилкобаламина, нуждается в SH-соединении, однако, в отличие от диолдегидратаз и других аналогичных ферментов, для проявления каталитической активности не требуются одновалентные катионы. Фермент высокоспецифичен в отношении структуры субстратов. Ни аналоги глутаминовой кислоты, ни аналоги β-метиласпарагиновой кислоты (как, например, β-этиласпартат) не являются субстратами мутазы.
О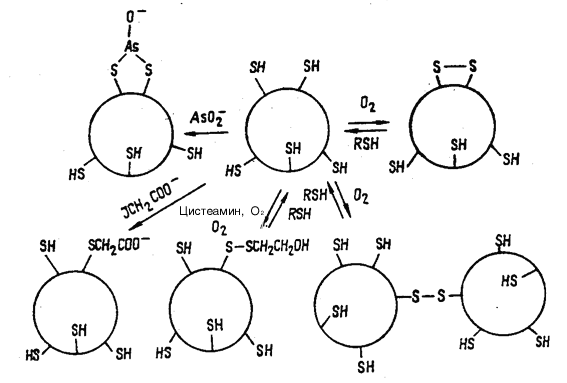
Схема 4. Схема доказательства наличия и роли SH-групп S-компонента глутаматмутазы.
пыты по очистке фермента позволили установить субъединичную структуру и этого аденозилкобаламин-зависимого фермента. Были получены в гомогенном состоянии две субъединицы, которые были названы S- и Е-белками. Каждый из белков не обладал порознь активностью. Рекомбинация их и взаимодействие с коферментом приводили к восстановлению активности. Первым был очищен Е-белок. Определение молекулярного веса показало, что это довольно большой белок с мол. массой около 128 000. В отличие от ферментов, рассмотренных выше, добавление Кобаламина не защищало Е-компонент глутаматмутазы от инактивации в растворе. Е-компонент связывал 1 моль аденозилкобаламина, а в присутствии семикратного избытка S-компонента дополнительно связывал еще один моль кофермента.
Компонент S после очистки, как оказалось, обладал намного меньшей мол. массой 17000 и, по-видимому, содержал важные для проявления ферментативной активности SH- группы. Титрование S-белка сульфгидрильными реагентами показало, что на 1 моль белка приходится пять SH-групп. Примечательной особенностью компонента была его способность к димеризации в присутствии О2. Расщепление димера осуществлялось обработкой последнего каким-либо RSH-соединением. Это свидетельствовало об образовании межмолекулярного дисульфидного мостика. Инактивация S-белка с помощью AsO2- доказывала наличие в активном центре по крайней мере одной из двух вицинальных тиольных групп. Превращение SH-групп S-белка представлены на схеме 3.
Метилмалонил-СоА-мутаза
Другой аденозилкобаламин-зависимый фермент, осуществляющий перегруппировку углеродного скелета метилмалонил-СоА в сукцинил-СоА был также сначала выделен из микроорганизмов, а затем из тканей млекопитающих. Оказалось, что этот кобаламин-зависимый фермент выполняет метаболически важную роль на пути превращения пропионил-СоА в сукцинил-СоА. Схема этого участка метаболизма включает 3 фермента: биотин-зависимую карбоксилазу, рацемазу, превращающую D-метилмалонил-СоА в L-изомер и рассматриваемую кобаламин-мутазу. После очистки метилмалонил-СоА-мутазы оказалось, что это субъединичный фермент с мол. массой 124000, расщепляющийся на два компонента с мол. массой 61 000 и 63000. Выделенная из печени овцы метилмалонил-СоА-мутаза представляет собой окрашеный в оранжевый цвет белок с мол. массой 165000. Фермент связывал 1 моль аденозилкобаламин на 75000.
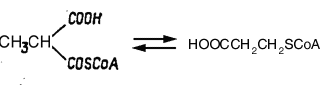
Рисунок 8. Превращение
метилмалонил-СоА в сукцинил-СоА.
2-метиленглутаратмутаза
С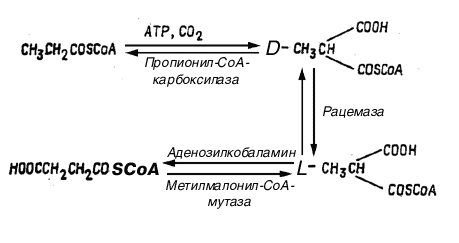
Схема 5. Схема превращения пропионил-СоА в сукцинил-СоА
ледующий сходный по действию Аденозилкобаламин-зависимый фермент-это 2-метиленглутаратмутаза, катализирующая обратимое превращение между 2-метиленглутаратом и 2-метилен-З-метилсукцинатом. Фермент был выделен из микробиологических источников при выращивании Clostridium на средах, содержащих никотиновую кислоту. Определение молекулярной массы частично очищенного препарата дало величину 170000. Обработка йодацетатом приводит к потере активности, что, очевидно, свидетельствует о наличии важных для катализа SH-групп. Действие AsО2-, однако, не выявило присутствия вицинальных дитиольных групп.Ферменты, трансформирующие α, ω-диаминокислоты
Еще одна группа аденозилкобаламин-зависимых ферментов была выявлена при исследовании микроорганизмов, растущих на L-лизине. Эти ферменты катализировали перенос NH2-гpyппы от концевого углеродного атома в диаминокислотах к соседнему атому углерода. Недавно описан аденозилкобаламин-зависимый фермент, который осуществляет перенос NH2-группы из α- в β-положение аминокислоты лейцина.
Рассмотрим более подробно аденозилкобаламин-зависимые ферменты, трансформирующие α, ω-диаминокислоты. Эти ферменты выделены из различных штаммов Clostridium.
Важно, что все три фермента в высшей степени специфичны для каждого из субстратов. Замена субстрата для данного фермента на субстраты других аминомутаз не позволяет осуществлять перенос аминогруппы.
D-α-Лизинмутаза выделена из С. sticklandi, мол. масса 250000. В процессе очистки фермента не происходило отщепления аденозилкобаламина, что свидетельствует о большой прочности связи комплекса апофермент-кофермент. Аналогично от L-β-лизинмутазы в процессе очистки аденозилкобаламин также не отделялся. Это тетрамерный фермент с мол. массой 160000; его субъединичная структура была подтверждена после того, как удалось выделить компоненты с мол. массой 32000 и 52000. Оказалось, что для обеспечения нормальной каталитической активности обеих мутаз необходим белок с мол. массой 60000. Как видно, аминомутазы сохраняют способность защищать в полностью реконструированном виде важные для биокатализа SH-группы. Это свойство характерно для большинства Аденозилкобаламин-ферментов.
Орнитинмутаза также представляет собой фермент с прочно связанным аденозилкобаламином, который не отщепляется при очистке. Очищенный фермент имел мол. массу 170 000 и диссоциировал на две субъединицы с мол. массой 90000. Этот фермент не требовал для своей активации какого-либо SH-белка, однако сам содержал важные для биокатализа SH-группы, вследствие чего ингибировался под действием тиоловых ингибиторов.
Заслуживает особого внимания прочность, с которой связан аденозилкобаламин во всех трех ферментах. При обработке их внутренним фактором ферменты инактивировались. Сравнительное исследование трех аминомутаз показало, что в дополнение к аденозилкобаламину для проявления их активности требуются: для D-α- и L-β-мутаз ионы Mg2+ и одновалентные катионы, причем для D-α-лизинмутазы-это К+, Rb+ и NH4+ (фермент ингибируется при добавлении Na+ и Li+). L-β-лизин-мутаза в разной степени активна в присутствии Li+, Na+, К+, Rb+, Cs+ и. NH4+. Для проявления активности орнитинмутазы добавления ионов металлов вообще не требуется.
Поразительное отличие аминомутаз от всех остальных кобаламин-зависимых ферментов состоит в том, что вторым обязательным коферментом для них является пиридоксальфосфат, который обеспечивает перенос ω-NH4-гpyппы в форме пиридоксамина или пиридоксальдимина. Очищенная орнитинмутаза неактивна до тех пор, пока к реакционной смеси не будет добавлен пиридоксальфосфат (PLP). Очевидно, что PLP входит в активный центр фермента и, по-видимому, связан в виде основания. Шиффа с ε-NН4-группой остатка лизина белка.
Рибонуклеотидредуктаза
Рибонуклеотидредуктаза - фермент, катализирующий конверсию рибонуклеотидов в 2`-дeзoкcиpибoнyклeoтиды. Этот фермент, имеющий ключевое значение для биосинтеза ДНК у большинства живых организмов, представляет собой железо-протеиновый комплекс, не зависящий от корриноидов. Однако ряд микроорганизмов и различные Euglenophyt содержат рибонуклеотидредуктазу, коферментом которой является аденозилкобаламин. Оказалось, что фермент состоит из одной полипептидной цепи с мол. массой 76000. Субстратом для рибонуклеотидредуктазы являются рибонуклеозидтрифосфаты. Для очищенной рибонуклеотидредуктазы необходимыми кофакторами, кроме аденозилкобаламина, являются тиолы.
Витамин В15
Получение и аналоги витамина В15
Впервые, как уже было упомянуто во введении, витамин В15 был обнаружен в экстракте печени быка.
Пангамовая кислота представляет собой эфир D-глюконовой кислоты и диметилглицина с молекулярной массой 281.
(СH3)2NCH2COOCH2(HCOH)4COOH
П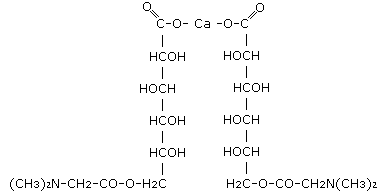
Рисунок 9. Пангамат кальция.
олучают пангамовую кислоту следующими двумя способами:Взаимодействием D-глюконолактона с монохлоруксусной кислотой и последующей обработкой продуктов реакции диметиламином.
Этерификацией глюконовой кислоты с диметилглицином. (выход около 25%)
Пространственное строение молекулы витамина В15 изображено на рис. 9 (Приведено строение пангамата кальция, соли, применяющейся в терапевтических целях)
Аналогами витамина В15 можно считать ряд соединений, представленных на рис. 10, так как во всех этих соединениях метильная группа лабильна, что и обуславливает биохимические свойства витамина В15.
Механизм действия
Потребность в витамине В15 (по Кребсу, данные от 1951 г.) составляет менее двух мг. в сутки. Однако принадлежность пангамовой кислоты к витаминам не доказана, в частности не существует достоверных сведений об авитаминозах или гипервитаминозах, связанных с этим соединением. Предпринимались попытки определить токсичность пангамовой кислоты в связи с ее широким применением в терапии. Выяснилось, что токсическая доза для витамина В15 приблизительно в 100000 раз превышает терапевтическую, т. е. вещество, фактически, безвредно.
Если кобаламиновые ферменты являлись в реакциях трансметилирования переносчиками метильной группы, то пангамовая кислота, судя по всему, выступает в этих реакциях в качестве донора одноуглеродного рацикала.
Лишь немногие вещества способны передавать СН3-группу другим молекулам. Среди них метионин, холин, бетаин и некоторые незаменимые аминокислоты.
В целом кажущаяся универсальность биологического действия витамина В15 (см. раздел «Клиника») обусловлена метилирующей способностью пангамовой кислоты и ее активностью в окислительных процессах.
К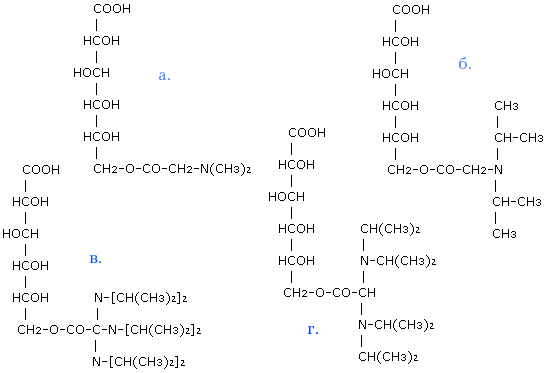
Рисунок 10. Гомологи пангамовой кислоты.
а) Глюконодиметиламиноацетат б) Глюконодиизопропиламиноацетат в) D-глюконотри-(N-диизопропиламино)-ацетат г) Глюконо-бис- (диизопропиламино)-ацетат
ак и витамин В12, пангамовая кислота принимает участие в реакциях синтеза метионина, холина, креатина, адреналина, стеринов и стероидных гормонов.
П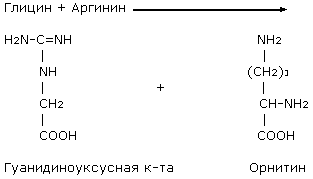
о
теории Борсука
и Дубнова синтез
креатина проходит
в две стадии.
На первой стадии,
которая проходит
в почках, из
аргинина и
глицина образуется
гуанидиноуксусная
кислота, затем
в печени гуанидиноуксусная
кислота подвергается
метилированию
(вторая стадия).
Последовательность
синтеза креатина
была подтверждена
опытами с изотопами
в работах Блоха
и Шенгеймера
(Bloch, Shoengheimer,
1941) и ряда других
исследователей.
Б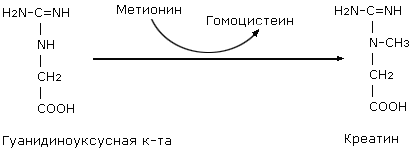
орсук
и Дубнов в опытах
in vitro
установили
высокую специфичность
креатинсинтезирующей
системы к метильному
донору (из 30
испытанных
аминов в реакцию
вступили лишь
метионин и
холин).
Способность пангамовой кислоты заменять в реакциях трансметилирования такой классический донор метильной группы, как метионин, вызывает у исследователей большой интерес.
Предположительно
характерными
для пангамовой
кислоты являются
реакции окислительного
деметилирования,
протекающие
аналогично
подобной реакции
саркозина.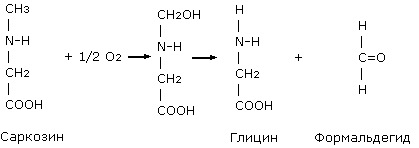
Образующийся
формальдегид
используется
затем в реакции
синтеза серина
или конденсируется
– в зависимости
от условий
ферментативного
процесса.
Описанный процесс начинается переносом атома водорода с саркозина (или диметилглицина) на саркозиндегидрогеназу (соотв., диметилглициндегидрогеназу), затем атом водорода передается флавопротеину, через него ферментам дыхательной цепи (цитохромы b, c, a, a3) и, наконец, кислороду. Стимуляция витамином В15 тканевого дыхания обусловлена, по всей видимости, именно этим процессом.
Клиника
Витамин В12
В качестве иллюстрации широты клинического применения витамина В12 можно привести выдержку из «Инструкции по применению витамина В12», утвержденной фармакологическим комитетом Ученого совета Минздрава СССР 29 июня 1955 года:
«Витамин В12 представляет собой кристаллическое вещество красного цвета, обладающее выраженным кроветворным действием в ничтожно малых дозах. Применение показано при следующих заболеваниях:
Болезнь Аддисон-Бирмера, включая случаи с нарушением функций нервной системы
Спру (тропическая и нетропическая формы)
Мегалобластическая анемия у детей
Рекомендуется испытать*:
Лучевая болезнь
Гиперхромная макроцитарная анемия
Анемии канкрозные
Анемии после резекции желудка
Анемии различного происхождения в предоперационном периоде.
Анемии макроцитарные гастроэнтерогенные
Острые хронические гепатиты и циррозы печени
Токсические анемии»
Вопрос о том, действует ли витамин В12 непосредственно на костный мозг, или его роль состоит лишь в активации фолиевой кислоты путем перевода ее в фолиновую.
В опытах Астальди, Вальдини и Фругони (1948), Томпсона (1952), Нивега (1953) с культурами тканей показали, что печеночные экстракты, также как и фолевая кислота в чистом виде, будучи добавлены к культуре костного мозга больных пернициозной анемией в стадии обострения способствуют ускорению вызревания мегалобластов и появлению нормобластов, в то время как кристаллический витамин В12 оказался неэффективен.
Витамин В15
Пангамовая кислота выпускается отечественными фармацевтическими предприятиями в виде кальциевой соли (пангамат кальция). Она активирует кислородный обмен, применяется при острых отравлениях алкоголем и другими наркотиками, при применении препаратов барбитуровой кислоты, салицилата натрия, ацетилхолина, кортизона, при отравлениях хлорсодержащими органическими соединениями и антибиотиками тетрациклинового ряда. Проявляет липотропный* эффект.
Липотропное действие проявилось при лечении гепатита и цирроза печени (алкогольного, сифилитического и иного происхождения). Этот эффект выражается в снижении содержания альбуминов и повышении до нормы содержания γ-глобулинов, усилении диуреза, увеличении содержания креатина в крови и моче, улучшении общего состояния: появлении бодрости, аппетита, нормализации сна, смягчении локальных симптомов. Применение пангамовой кислоты также стабилизирует деятельность системы гипофиз-надпочечники и центральной нервной.
Активирует кислородный обмен, участвует в окислительных процессах. Улучшает трофику сердечной мышцы в результате стимуляции биосинтеза креатина и креатинфосфата и активации ферментов дыхательной цепи. Оказывает положительное влияние при кислородном голодании токсической природы. Существенно повышает активность дегидразы при некотором снижении активности цитохромоксидазы (вышеупомянутый цитохром а3). Снижение активности цитохромоксидазы связывают со снижением напряженности переноса кислорода через систему цитохром-цитохромоксидаза. (Функция последней сводится к катализу реакции между кислородом и восстановленной формой последнего цитохрома). А. В. Докукин, З. С. Константинова, Ю. С. Чечулин и Ю. В. Букин обнаружили отчетливо выраженное защитное действие при локальной гипоксии сердца: кошкам перевязывали левую коронарную артерию. У тех из них, которым давали заблаговременно витамин В15 аритмия и фибрилляция возникали в среднем через 10,6 минуты, в то время как у контрольных животных уже через 3,8 минуты.
Противотоксическое действие пангамовой кислоты объясняется ее вероятным участием в биосинтезе холина, который связывает и выводит токсические вещества и/или стимуляцией окисления токсических субстратов. Были получены положительные результаты при лечении больных с хроническим алкоголизмом (по мнению Н. К. Гудковой и З. Л. Синкевич, применение витамина В15 способно заменить традиционный курс лечения), различными наркоманиями (кодеиномания, морфинизм, гашишизм и др.). Отмечается исчезновение влечения к наркотику и регресс соматических изменений (цирроза, сердечно-сосудистых заболеваний, гепатита).
Существует опыт применения пангамовой кислоты у детей с олигофренией в стадии выраженной дебильности. Лишь в трех из 15-ти случаев не наблюдалось улучшения речи, лишь в шести – интеллектуальной деятельности, лишь в двух случаях не происходило улучшения общего психического состояния. Было отмечено выраженное стимулирующее воздействие на функциональную активность мозга, было указано на возможность применения пангамата кальция в психиатрической клинике.
Заключение
Довольно!
Чтение принесло свои плоды: в голове у меня все спуталось
окончательно и я мгновенно убедился, что не понимаю ничего…
Михаил Булгаков, «Записки юного врача»
Витамины В12 и В15 играют в организме важную роль, причем в некоторых биохимических процессах они могут принимать совместное участие (например, в реакциях трансметилирования). Хотя большая часть данного реферата посвящена витамину В12, я стремился по возможности подчеркнуть возможности совместного участия этих витаминов в биологических реакциях.
Все же главная задача, поставленная передо мной, заключалась в возможно более полном изложении химических свойств цианкобаламина и пангамовой кислоты и рассмотрении конкретных процессов, проходящих в организме с их участием.
Поэтому при подборе литературы я руководствовался стремлением сконцентрировать внимание именно на химических данных, а не на клинических исследованиях биологической активности этих веществ. В связи с этим нельзя не отметить того, что большая часть литературы, которую можно встретить в библиотечных каталогах, посвящена именно клиническим аспектам. Впрочем, клинические данные также не были обойдены вниманием при написании реферата.
Мною были использованы как источники труды, принадлежащие перу исследователей, стоявших у истоков изучения витаминов В12 и В15 (в частности Лестера Смита) или посвятивших значительную часть своей жизни вопросам, связанным с их участием в биохимических процессах (как И. Н. Гаркина). В таких работах я обнаружил не только достаточное количество научных сведений по интересующему меня вопросу, но и живой интерес авторов к обсуждаемой теме, выливающийся в увлекательный и весьма, поэтому, убедительный стиль изложения материала. Это существенно облегчило написание данного реферата.
В связи с тем, что рассматриваемые вещества имеют весьма сложную структуру, а обозначения их, видимо, еще не устоялись окончательно, возникали сложности при рассмотрении разных источников, в которых одни и те же вещества могли быть обозначены по-разному, а так как в некоторых статьях мне не удалось найти расшифровки химических сокращений, оказалось необходимо дополнительно широко использовать справочную литературу.
За время работы над рефератом я получил достаточно большой объем знаний не только о цианкобаламине и пангамовой кислоте, а это достаточно специфическая информация, но и по менее конкретным вопросам, таким как общие закономерности взаимодействия организма с биологически активными веществами, биохимические методы исследования и др. Самое большое впечатление на меня произвела колоссальная сложность человеческого организма как системы, в которой сосуществует и взаимодействует не поддающееся на первый взгляд осмыслению количество различных веществ, а также то, сколько еще загадок предстоит разрешить человечеству прежде, чем оно придет хотя бы к удовлетворительному пониманию биохимических закономерностей.
Список использованной литературы
Лестер Смит «Витамин В12», Москва, изд. Иностранной Литературы, 1962 г.
А. М. Юркевич, И. П. Рудакова «Структура, свойства и механизм действия кобаламиновых коферментов», серия «Итоги науки и техники: биоорганическая химия», т. 5, Москва, ВИНИТИ, 1985
В. М. Березовский «Химия витаминов», Москва, «Пищевая промышленность», 1973 г.
Т. Т. Березов, Б. Ф. Коровкин «Биологическая химия», Москва, «Медицина», 1992 г.
А. Л. Ленинджер «Основы биохимии», Москва, «Мир», 1985
«Витамин В12 и его клиническое применение», Москва, «Медицина», 1956 г.
Паханцева Е. С., Пчелкина В. В., Сыромятников Е. Ю. «Кобамидные ферменты и их роль в реакциях трансметилирования», журн. «Витамины», вып. 7, Киев, «Наукова думка», 1973 г.
И. Н. Гаркина «Пангамовая кислота и ее производные», Москва, Институт Биохимии имени А. Н. Баха, 1965 г.
И. Н. Гаркина «Вопросы медицинской химии», Москва, 1962 г.
Большая Советская Энциклопедия, Москва, «Советская Энциклопедия», 1962 г.
Дополнительно:
И. В. Стрельчук «О лечении хронического алкоголизма и других наркоманий витамином В15», Москва, НИИ Судебной Психиатрии им. Сербского, 1962 г.
М. Г. Блюмина, Т. К. Белякова «Опыт применения витамина В15 при олигофрении у детей дошкольного возраста», Москва, 1963 г.
* Известная качественная реакция на α-аминокислоты, дающая интенсивное фиолетовое окрашивание.
* ТГФК – тетрагидрофолевая кислота.
* Здесь список заболеваний процитирован не полностью
* Т. е. предотвращает жировую инфильтрацию печени. Инфильтрация – скопление в ткани клеточных элементов в смеси с кровью и лимфой.
35