Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
Психология и педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Рефераты по сексологии
Рефераты по информатике программированию
Краткое содержание произведений
Реферат: Курсовая работа по органической химии
Реферат: Курсовая работа по органической химии
Министерство образования российской федерации
Самарский государственный университет
Химический факультет
Кафедра органической химии
Специализация органическая химия
СИНТЕЗ 5`-Р-(ДИАМИНОАДАМАНТИЛ)- 2`,3`-О-ИЗОПРОПИЛИДЕНАДЕНОЗИН-МОНОФОСФАТА
Курсовая работа
Выполнила студентка
4 курса 441 группы
Зенина Наталья Ивановна
________________________
Научный руководитель д.х.н.
проф. Пурыгин П.П.
________________________
Работа защищена
²_____²____________2003 г.
Оценка__________________
Зав. каф. ОХ д.х.н.
проф. Пурыгин П.П.
________________________
Самара
2003
СОДЕРЖАНИЕ
| 1. Введение | 3 |
| 2. Обзор литературы | 4 |
| 2.1. Перспективы использования адамантана | 4 |
| 2.2.Фармакологические свойства адамантана | 5 |
| 2.3. Клиническое применение производных адамантана | 5 |
| 2.4. Противовирусная активность производных адамантана | 8 |
| 2.5. Противоспидовая активность производных адамантана | 9 |
| 2.6. Противоопухолевая активность производных адамантана | 13 |
| 2.7. Другие биологически активные производные адамантана | 14 |
| 2.8. Синтез адамантансодержащих соединений включающих пуриновые и пиримидиновые кольца | 16 |
| 3. Экспериментальная часть | 19 |
| 3.1. Реагенты и оборудование | 19 |
| 3.2. Синтез 2`,3`-о-изопропилиденаденозина | 19 |
| 3.3. Синтез 5`-р-(дихлор) -2`,3`-о-изопропилиденаденозинмонофосфата | 20 |
| 3.4. Синтез аминоадамантана | 20 |
| 3.5 Синтез 5`-р-(диаминоадамантил)- 2`,3`-о-изопропилиденаденозин-монофосфата | 21 |
| 4. Обсуждение результатов | 22 |
| 5. Вывод | 26 |
| 6. Список использованных источников | 27 |
1.ВВЕДЕНИЕ
Актуальность работы: В современной химии одной из актуальных проблем является синтез биологически активных производных адамантана, которые в дальнейшем могут быть использованы как лекарственные препараты при лечении онкологических больных в том числе и ВИЧ-инфицированных.
Целью данной работы является синтез модифицированного нуклеозида по углеводной части молекулы, к которым в последние десятилетия сильно возрос интерес, как к потенциальным противоопухолевым и противовирусным препаратам.
Практическая ценность работы состоит в получении нового производного адамантана, биологическая активность которого обусловлена особенностями структуры адамантана, его симметрией, большим объемом и значительной липофильностью молекулы. Так уже в 70-е гг. XX в. в медицине широко использовали аминопроизводные адамантана, обладающие противовирусной активностью в отношении штаммов вирусов гриппа А и В [1].
Научная новизна: Показана принципиальная возможность получения 5`-р-(диаминоадамантил)-о-изопропилиденаденозинмонофосфата.
2. ОБЗОР ЛИТЕРАТУРЫ
2.1. ПЕРСПЕКТИВЫ ИСПОЛЬЗОВАНИЯ АДАМАНТАНА
Химия адамантана и его производных является сравнительно молодым разделом органической химии (со времени обнаружения адамантана в нефтях прошло примерно 70 лет). В то же время, наблюдается постоянный рост числа исследований в этой области, особенно начиная с 70-х годов ХХ столетия. Одной из причин этого является перспективность практического использования его производных.
На основе адамантана получают алмазоподобные пленки (свое название адамантан получил от греческого “непобедимый” – греческое название алмаза), по своей твердости лишь в 3 раза уступающие алмазу. Они были получены из паров адамантана при наложении двух видов электрического разряда – тлеющего и высокочастотного.
Алкиладамантаны используют как углеводородное реактивное топливо. Масла, полученные на основе алкиладамантанов обладают термостойкостью, низким индексом вязкости, поэтому их рекомендуют использовать в качестве кабельного масла. Также алкиладамантаны обладают бактерицидным действием, вследствие чего рекомендовано использовать их в качестве антимикробных присадок к смазочным материалам.
Известно, что Управление вооружений армий США намеревалось провести испытания нового взрывчатого вещества – 1,3,5,7-тетранитроадамантана, обладающего высокой стойкостью к ударным нагрузкам и в то же время по эффективности превосходящего “классический” тол.[2]
Перфторированный адамантан применяется в качестве компонента искусственной крови. [3]
2.2. ФАРМОКОЛОГИЧЕСКИЕ СВОЙСТВА АДАМАНТАНА
Высокая липофильность и объемная структура адамантильного радикала при его введении в молекулы различных биологически активных соединений в значительной мере модифицирует их фармакологическое действие. Таким образом была модифицирована структура ряда антимикробных, противоопухолевых, иммунодепрессивных, гормональных, аналгетических, противовоспалительных, нейротропных средств. [133] Так введение адамантила в 1-β-D-арабинофуранозил, цитозин привело к пролонгированию эффекта полученного соединения. При этом молекулярный механизм действия этого вещества не изменяется, так как для проявления им цитостатической активности требуется гидролиз и освобождение от адамантана. Присоединение адамантильного радикала к пуриновому антиметаболиту 6- тиоинозину также усилило иммуносупрессивную активность производного по сравнению с исходным соединением. [4]
Предполагают, что модификация биологической активности связана с изменением пространственного строения, гидрофобности и липофильности соединений, более благоприятными условиями их транспорта через биологические мембраны. [3]
На данный момент синтезировано более 1000 новых производных адамантана, в том числе и по мостиковому положению. Фармакологическое изучение показало наличие среди них веществ, обладающих выраженной психотропной, курареподобной, иммунотропной, противовирусной, антикаталептической, противоаллергической активностями, а также соединений, влияющих на ферментативную систему печени. [5]
2.3. КЛИНИЧЕСКОЕ ПРИМЕНЕНИЕ ПРОИЗВОДНЫХ АДАМАНТАНА
Введение в адамантан в положение 1 или 3 различных заместителей приводит к тому, что его можно использовать во многих областях медицины. Еще в 1966 г. в медицинскую практику был введен гидрохлорид 1-аминоадамантана в качестве антивирусного средства. В медецине это соелинение часто называют мидантаном или амантадином, но фирменное название симметрел: [2]
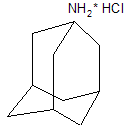
Изначально его применяли только как антигриппозный препарат. В настоящее же время мидантан наиболее часто используется в неврологической клинике для лечения болезни Паркинсона и паркинсонического синдрома (паркинсонизм является одним из наиболее распространенных заболеваний центральной нервной системы и встречается у 1-2,5% людей, причем риск заболевания с возрастом увеличивается). [4]
Механизм действия симметрела состоит в том, что он не убивает вирусы, а лишь блокирует их проникновение в клетку, вследствие чего он особенно эффективен для профилактики и на ранних этапах заболевания. Имеется, однако, другая точка зрения на механизм действия препарата, согласно которой аминоадамантан и его производные “вмешиваются” в ранние этапы репродукции вирусов, а их ингибирующее действие связано с латентным периодом – началом репликации и синтеза вирусспецифических РНК. [2]
В качестве других средств против заболеваний центральной нервной системы в клинике прошли испытания бемантан (I) (2-(N-бензоиламино)адамантан), димантан (II) (2,2`-ди(адамантил)амин гидрохлорид), кемантан (III) (1-гидроксиадамантан-4-он), адапромин (IV) (2-этил-1-адамантанметиламина гидрохлорид) и мемантин (V) (1,3-диметил-5-аминоадамантана). [4]
|
|
Бемантан |
|
|
Димантан |
|
|
Кемантан |
|
|
Адапромин |
|
|
Мемантин |
|
|
Ремантадин |
В медицине широко используется ремантадин (VI) (2-метил-1-адамантанметиламина гидрохлорид) как антигриппозное лекарственное вещество. [2] Помимо этого ремантадин ингибирует репродукцию вируса Синдбис из-за того, что он как липофильное слабое основание способен повышать рН эндосомального содержимого и препятствует депротенизации вируса. [6]
2.4. ПРОТИВОВИРУСНАЯ АКТИВНОСТЬ АДАМАНТАНА
Среди вирусных инфекций грипп и другие острые заболевания дыхательных путей, вызываемые РНК-содержащими вирусами, занимают ведущее место. Поскольку стадии размножения вируса в зараженной клетке еще до конца не изучены, то трудно сказать с каким именно процессом связано противовирусное действие активных производных адамантана. Однако установлено, что производные адамантана не влияют на адсорбцию вирусных частиц на поверхности чувствительных клеток и проникновение вируса в клетку [7].
Как уже упоминалось, антивирусной активностью обладают аминопроизводные адамантана (ремантадин и симметрел). Механизм их действия связан с блокированием функции ионных каналов клетки или белка вируса группы А. В институте нефтехимического синтеза были разработаны новые лекарственные вещества, которые ингибировали репродукцию вирусов гриппа А и В, а также вирусов простого герпеса. Эти лекарственные вещества представляют собой комплексные препараты адамантанов и полимерных матриц (поликарбоксилаты анионного типа на основе малеинового ангидрида и дивинилового спирта). Данные соединения обладают токсичностью в 5-10 раз ниже, чем у ремантадина [8].
Также осуществлена трехкомпонентная конденсация инозиндиальдегида, пропандиенфосфонистой кислоты и 1-аминометиладамантана, приведшая к образованию 9-[(1`,4`-морфолил)-3`-окси-N`-(1-адамантилалкил)-5`-пропандиенфосфинат-6`-оксиметил-2`]-гипоксантинов, обладающих противовирусной активностью в отношении РНК и ДНК-содержащих инфекционных и онкогенных вирусов [3].
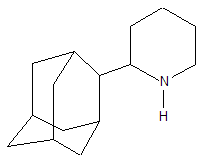
Из литературных данных известно, что одним из лекарственных средств против вируса гриппа А и В является 2-(адамант-2-ил) пиперидин [9]:
2.5. ПРОТИВОСПИДОВАЯ АКТИВНОСТЬ ПРОИЗВОДНЫХ
АДАМАНТАНА
Число людей заразившихся и умерших от СПИДа постоянно возрастает, лекарственные вещества не всегда эффективны. По этим причинам актуально использовать в качестве иммунорегуляторов, в частности, для борьбы с вирусом СПИДа, аминоадамантановые производные следующей формулы:
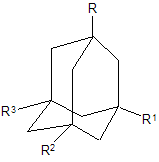
где R-R3=H, арил, гетерофил, замещенный или незамещенный NH2, алкил, алкенил, алкинил [10].
Анти-ВИЧ-активностью обладает также кемантан (III). Это было показано в экспериментах с использованием ВИЧ-инфицированных человеческих МТ-4 лимфобластодных клеток. Кемантан при добавлении в культуру указанных клеток после их заражения вирусом, обладал анти-ВИЧ-активностью в широком диапазоне концентраций. При концентрации 500 мкг/мл он ингибировал экспрессию вирусных протеинов на поверхности инфицированных клеток на 50%. При этом наблюдалось уменьшение (на 30% по сравнению с контролем) выхода растворимых ВИЧ-антигенов в культурную среду [11].
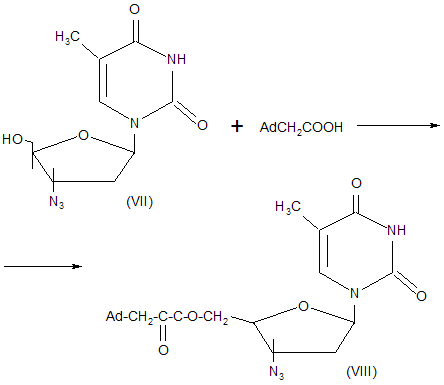
Японские исследователи разработали метод синтеза производных 3`-азидо-3`-дезокситимидина содержащих фрагмент адамантана в положении 5`-нуклеозида. Изучение биологического действия сложного эфира (VIII), полученного из азидотимидина (VII) и (1-адамантил)-уксусной кислоты, показало, что его концентрация в паренхиматозной ткани головного мозга в 18 раз превышает величину, полученную в сравнительном эксперименте с 3`-азидо-3`-дезокситимидином. Следовательно, введение фрагмента адамантана в 3`-азидо-3`-дезокситимидин облегчает транспорт этого лекарственного средства в ткани головного мозга, куда проникает вирус СПИДа и поражает центральную нервную систему.
Схема 1.
С целью поиска новых антиспидовых препаратов осуществлен синтез 3`-(1-адамантил) тиоуреидопроизводного тимидина (Х) взаимодействием 3`-аминотимидина (IX) с (1-адамантилфосфонил) фосфата (XI) с монофосфатом азидотимидина (XII) [3].
Схема 2.
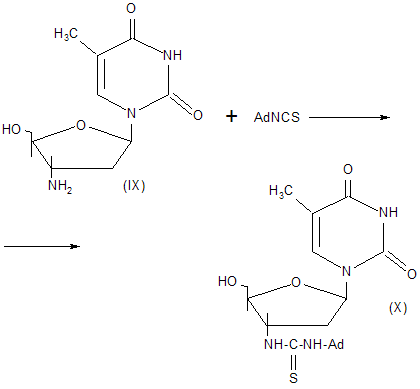
Схема 3.
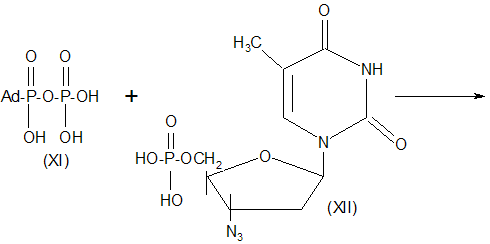
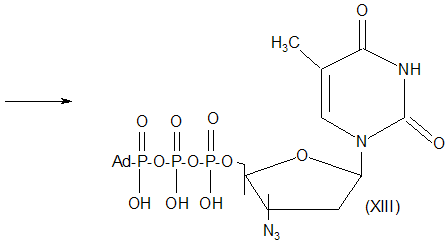
Патентуют использовать в качестве противовирусноактивных соединений, в том числе в отношении ВИЧ, полимерные аналоги адамантана.
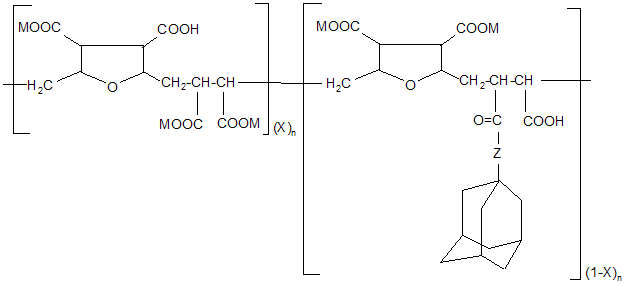 где n=30-50
где n=30-50
x=0,1-0,25
M=H, NH2, щелочные металлы
Z=группа ab
a= NH, O
b=C1-C8 алкилен [12].
2.6. ПРОТИВООПУХОЛЕВАЯ АКТИВНОСТЬ ПРОИЗВОДНЫХ
АДАМАНТАНА
Патентуют способ лечения рака путем вызывания апоптоза раковых клеток с помощью соединений формулы:
|
|
|
|
|
|
|
|
где W=CH2, O, S, SO, SO2
R1=H, галоген, алкил
R2=ОН, замещенный алкил, незамещенный алкил
R3=Н, ОН, алкил, алкокси
R4=Н, алкил, галоген, алкоксил
R5=галоген, замещенный алкил, незамещенный алкил
R6=Н, ОН, галоген, алкокси
R7=Н, галоген
R8=Н, галоген, алкил
R9=Н, ОН, галоген
Y=алкил, алкилен, О, С=N
|
NH2
Z=N, CH
X=Q, Q1, Q2. [13]
Противоопухолевая активность среди адамантанзамещенных фософорилированных нуклеозидов найдена у 5`-o-(1-адамантилалкил)фосфорилпроизводных 1-β-D-арабинофуранозилцитозина [3].
Сложные эфиры адамантанкарбоновой кислоты и некоторые нуклеотиды общего строения
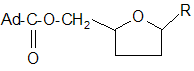
(где R=6-азаурацил, 6-меркаптопурил, аденин, гипоксантин) проявляют антиопухолевую активность.[14]
2.7. ДРУГИЕ БИОЛОГИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ
АДАМАНТАНА
Замещенные амиды адамантанкарбоновой кислоты могут служить снотворными средствами. Введение адамантильного остатка в 2-оксинафтохинон приводит к получению антималярийных препаратов. [14]
Адамантиламиноспирты и их соли обладают выраженным психостимулирующим действием и при этом мало токсичны. [15]
Некоторые N-(адамант-2-ил)анилины проявляют нейротропную активность [16], а биологическая активность N-(адамант-2-ил)гексаметиленимина проявляется по отношению к паркинсоническому синдрому [17].
В качестве иммунодепрессантов и как противовоспалительные средства предлагается включать в состав лекарственных препаратов соединения следующего строения:
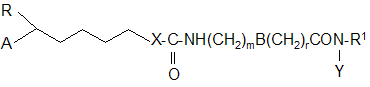
где R=H, Ph
R1=H, алкил
А=адамантил
Х=О
Y=ОН
Извилистая линия обозначает С1-С5
В=фениленовое или циклогексиленовое кольцо. [18]
Предложен способ лечения лейкемии и других заболеваний, связанных с недостаточностью функций ионотропных ацетилхолиновых рецепторов. Способ основан на использовании лекарственных форм, содержащих производные адамантана следующей структуры:
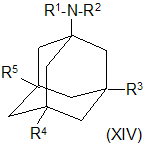
где R1 и R2=H, алкил, или вместе с атомом азота образуют гетероциклическое кольцо.
R3 и R4 =Н, алкил, циклоалкил или фенил
R5=Н или фенил [19].
Из литературных данных известно, что данные вещества могут быть использованы как лекарственные средства для борьбы с нейродегенеративными заболеваниями мозга человека и животных, в частности, вызываемых белками – прионами (заболевание скрапия). Данные белки вызывают гибель нейронов. Производные адамантана типа (XIV) ингибируют действие этих белков [20].
Кроме того алкильные производные аминоадамантана схожие по строению с соединениями типа (XIV) могут применяться для лечения заболеваний внутреннего уха и шума в ушах [21].
2.8. СИНТЕЗ АДАМАНТАНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
ВКЛЮЧАЮЩИХ ПУРИНОВЫЕ И ПИРИМИДИНОВЫЕ КОЛЬЦА
Высокая биологическая активность и малая изученность производных адамантана приводит к высокому интересу по синтезам новых производных адамантана. Так реакцией присоединения 1,3-дегидроадамантана к 2-метилпиридину (2-пиколину) был получен 2-(адаман-1-илметил)пиридин [22]. Патентуется способ получения 5-[3(4)-R-1-адамантил]-пиримидинов общей формулы:
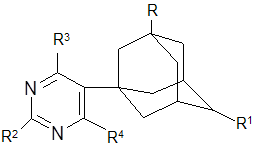
где R, R1=Н, Рh, низший алкил.
R1, R2, R3, R4=Н, ОН, NН2, галоген.
Данные соединения были получены взаимодействием адамантанола-1 с соответствующим пиримидиновым основанием в среде трифторуксусной кислоты при молярном соотношении адамантанол : пиримидиновое основание : трифторуксусная кислота 1 : 1 : 6 [23].
Преображенской и сотрудниками было осуществлено взаимодействие уридина с дихлорангидрином 1-адамантилфосфоновой кислоты в пиримидине. В результате получили неразделимую смесь двух веществ [4]. Дальнейшие исследования показали, по данным ЯМР, масс-спектроскопии и отсутствию подвижности при электрофорезе на бумаге в фосфатно-щелочном (рН 7,7) и боратном (рН 9,2) буферах, полученные соединения являются изомерными цикло-(1-адамантил)фосфонатами уридина (IIa) и (IIIa):
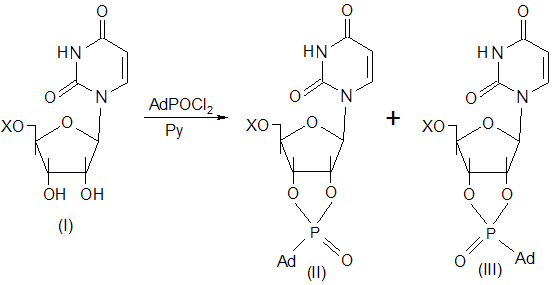
где X=OH – a
X=OAc – б
Х=F – в
Аналогичные соединения образовывались при взаимодействии 5`-о-ацетилуридина и 5`-фтор-5`-дезоксиуридина с дихлорангидридом 1-адамантилфосфоновой кислоты. Однако реакция с 2`,3`-о-изопропилиденуридином в этих же условиях не пошла [25]. Смесь диастереомерных по фосфору соединений получается также при взаимодействии 5-бром-, 5-фтор-, 6-азауридина или их 5`-о-производных с дихлорангидридом 1-адамантилфосфоновой кислоты [26].
При взаимодействии дихлорангидрида 1-адамантилфосфоновой кислоты с пуриновыми основаниями получается многокомпонентная смесь с большим содержанием исходного нуклеозида. Однако реакция идет по той же схеме с образованием диастереомерных соединений:
|
|
|
|
| (I а-г) | (II а-г) R-изомер | (III а-г) S-изомер |
где а: R=Н, R`=NН2;
б: R=Ac, R`=NH2;
в: R=H, R`=SCH3;
г: R=Tr, R`= SCH3.
Количество R-изомера в 2,5-3 раза больше количества S-изомера [27].
3. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
3.1. РЕАГЕНТЫ И ОБОРУДОВАНИЕ
Перемешивание аденозина с ацетоном, концентрированной серной кислотой и безводным сульфатом меди проводили на магнитной мешалке.
Упаривание всех растворов поводили на роторном испарителе "Rotodest" под вакуумом 15-20 мм. рт. ст.
Инфракрасный спектр синтезированного соединения регистрировали на спектрометре "ИКС-29", в таблетках из KBr.
В качестве реагентов были использованы
1) высушенный аденозин;
2) абсолютированный ацетон;
3) прокаленный сульфат меди;
4) концентрированная серная кислота;
5) триэтилфосфат;
6) треххлористая окись фосфора;
7) сухой гидроксид кальция;
8) водный раствор гидроксида аммония;
9) вода;
10) бензол;
11) эфир;
12) абсолютированный хлороформ;
13) сухой гидроксид натрия;
14) гидрохлорид аминоадамантана.
3.2. СИНТЕЗ 2`,3`-О-ИЗОПРОПИЛИДЕНАДЕНОЗИНА
0,4 г (1,5∙103 моль) аденазина высушивали в пистолете Фишера в течение 10-12 ч при 100 0С (в парах толуола над пятиокисью фосфора) и готовили суспензию с 40 мл ацетона, добавляли 2 г (1,25∙10-2 моль) безводного сульфата меди и 0,01 мл концентрированной серной кислоты. Суспензию перемешивали 48 ч при 38 0С. Осадок отделяли, промывали 2-3 раза небольшим количеством ацетона и объединенный фильтрат встряхивали в течение 1 ч с 0,4 г сухого гидроксида кальция. Осадок отфильтровывали и промывали ацетоном 2 раза по 10 мл. Фильтрат упаривали досуха. Выход продукта составил 0,21 г (52% от теоретического), белые кристаллы, t.пл. 218-220 0С (лит 220-222 0С) [26].
3.3. ПОЛУЧЕНИЕ 5`-Р-(ДИХЛОР)-2`,3`-О-ИЗОПРОПИЛИДЕНАДЕНОЗИНМОНОФОСФАТА
Охлаждали до 0 0С раствор треххлористой окиси фосфора (0,15 мл) в триэтилфосфате (8 мл) добавляли 2`,3`-о-изопропилиденаденозина (0,75∙10-3 моль). Смесь выдерживали 24 ч при 4 0С и затем нейтрализовали 25% водным раствором гидроксида аммония и оставляли на 1 ч при 4 0С. Затем добавляли воду (20 мл), смесь экстрагировали бензолом (10 мл), а затем эфиром (2 х 10 мл). Водный слой отделяли, упаривали досуха и растворяли в воде (80 мл). Нуклеотид выделяем ионнообменной хроматографией на колонке (2,5 х 10 см), неподвижная фаза – Дауэкс-50 (Н+), роль подвижной фазы выполняет вода. Собирали частицы, поглощающие в УФ-области. Объединяли, упариваем досуха, соупаривали с 10% водным раствором гидроксида аммония (6 мл) растворяли в воде (10 мл) и подвергали сухой заморозке. Выход составил 0,126 г (60% от теоретического) [29].
3.4. СИНТЕЗ АМИНОАДАМАНТАНА
К водному раствору 1,87 г (1 моль) гидрохлорида аминоадамантана добавляли 0,40 г (1 моль) NaOH. Смесь экстрагировали эфиром (2 х 15 мл). Органический слой отделяли и выпаривали досуха. Выход аминоадамантана 1,83 г (98%), t.пл.=210 0С.
3.5. СИНТЕЗ 5`-Р-(ДИАМИНОАДАМАНТИЛ)-2`,3`-О-ИЗОПРОПИЛИДЕНАДЕНОЗИНМОНО-ФОСФАТА
К полученному 5`-р-(дихлор)аденозинмонофосфату добавили 0,585 г раствора аминоадамантана в 2 мл абсолютного хлороформа. Осадок отфильтровывали. Фильтрат упаривали. Выход продукта составил 0,065 г (52% от теоретического).
4. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Синтез 2`,3`-о-изопропилиденаденозина осуществлялся взаимодействием аденозина с ацетоном в среде абсолютного ацетона при постоянном перемешивании. Схема этой реакции такова:
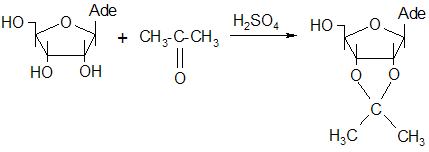
Предполагаемый механизм этой реакции следующий [29]:
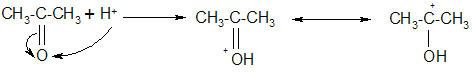
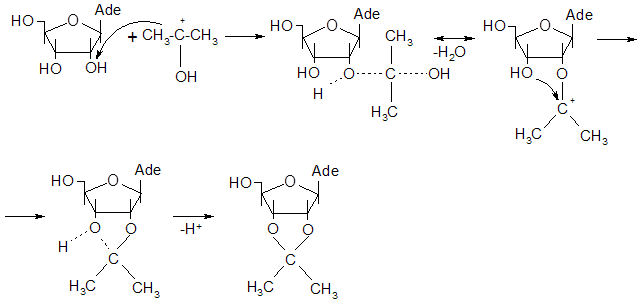
Синтез 5`-р-(дихлор)-2`,3`-о-изопропилиденаденозинмонофосфата осуществлялся взаимодействием 2`,3`-о-изопропилиденаденозина с треххлорокисью фосфора в присутствии водного раствора гидроксида аммония по следующей схеме:
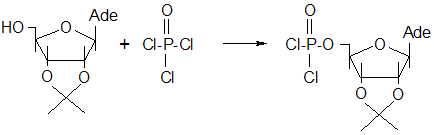
Предполагаемый механизм этой реакции следующий:

Синтез аминоадамантана осуществлен реакцией нейтрализации гидрохлорида аминоадамантана гидроксидом натрия по следующей схеме:
![]()
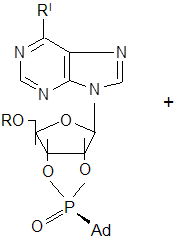
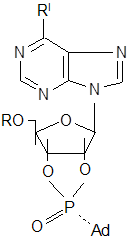
Синтез 5`-р-(диаминоадамантил)- 2`,3`-о-изопропилиденаденозинмоно-фосфата осуществлялся взаимодействием аминоадамантана с 5`-р-(дихлор)-2`,3`-о-изопропилиденаденозинмонофосфатом. Схема этой реакции такова:

Предполагаемый механизм этой реакции следующий [30]:
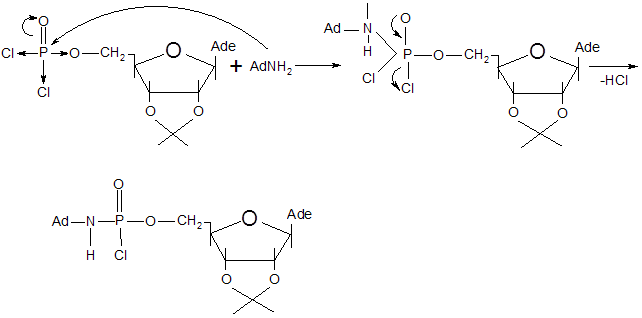

Чистота 5`-р-(диаминоадамантил)-2`,3`-о-изопропилиденаденозинмонофосфата была доказана методом ТСХ в системе бутанол : вода : уксусная кислота – 5:3:2 Rf=0,78 при УФ проявлении.
Наличие адамантильного остатка подтверждено ИК-спектроскопией. В ИК-спектре прослеживаются полосы, характерные для С-С (800 см-1, 970 см-1), Н-С-С (1155 см-1, 1350 см-1), Н-С-Н (1453 см-1, 2853 см-1), С-С-С (2907 см-1, 2933 см-1) адамантильного ядра и P-N (890 см-1).
5. ВЫВОДЫ
1. Показана принципиальная схема получения 5`-р-(диаминоадамантил)-2`,3`-о-изопропилиденаденозинмонофосфата взаимодействием аминоадамантана и 5`-р-(дихлор)-2`,3`-о-изопропилиденаденозинмонофосфата.
2. Чистота синтезированного соединения доказана методом ТСХ. Структура доказана методами ИК-спектроскопии.
6. СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Касьян Л.И., Касьян А.О., Голодаева Е.А. // журн. органич. химии. 2000. т.36. №12. с. 1776-1779.
2. Багрин Е.И. Адамантаны: получение, свойства, применение. М.:Наука, 1989. 264 с.
3. Литвинов В.П. //Химия гетероциклических соединений. 2002. №1. с. 12-39
4. Морозов И.С., Петров В.И., Сергеева С.А. Фармакология адамантанов. Волгоград: Волгоградская мед. академия, 2001. 320 с.
5. РЖ Химия. 2000. 10. 19029.
6. Андронова В.Л. // Антибиотики и химотерапия. 1996. т.41. №718. с. 26-30.
7. Механизмы антивирусного действия производных адамантана / Под ред. М.К. Индугена. Рига: Зинатне, 1981.
8. РЖ Химия 2001. 10. 19067К.
9. РЖ Химия 2002. 15. 19061.
10. Патент 6255348 США // РЖ Химия 2002. 15. 19042П.
11. Ковалев И.Е., Щипулина Н.В. // Доклады Российской академии наук. 2001. т. 378. №6. с. 819-822.
12. Заявка 99102174/14 Россия // РЖ Химия 2001. 11. 19053П.
14. Севастьянова В.В., Краюшкин М.М., Юрченко А.Г. // Успехи химии. 1970. т. 39. вып. 10. с. 1721-1753.
15. IX Международная научная конференция по химии и технологии каркасных соединений // Нефтехимия. 2001. т. 41. №6. с. 478-480.
16. РЖ Химия 1998. 22. Ж 195.
17. РЖ Химия 2000. 06. 190359.
18. Заявка 98122430/ Россия // РЖ Химия 2001. 11. 19047П.
19. Заявка 1201234 ЕАВ // РЖ Химия. 2002. 20. 190241П.
20. Заявка 4229805 ФРГ // РЖ Химия. 1996. 16. 0230П.
21. Заявка 19528388 Германия // РЖ Химия. 1999. 01. 0345П.
22. РЖ Химия. 2002. 17. 19Ж95.
23. Патент 2064930 Россия // РЖ Химия. 1997. 13Н. 87П
24. Преображенская М.Н., Мельник С.Я., Олейник Д.М., Шепелев Е.С., Турчин К.Ф., Санин П.И. // Биоорганическая химия. 1975. т.1. №2. с. 277-278.
25. Преображенская М.Н., Мельник С.Я., Олейник Д.М., Шепелев Е.С., Турчин К.Ф., Санин П.И. // Биоорганическая химия. 1975. т.2. №5. с. 627-631.
26. M.N. Preobrazhenskaya, S.Ya. Melnik, D.M. Oleinik, E.S. Shepelev, P.I. Sanin // Carb. Nucleosides, Nucleotides. 1975. т.2. №2. с. 413.
27. Недоаезова Т.П., Мельник С.Я., Ярцева И.В., Преображенская М.Н. // Биоорганическая химия. 1978. т.4. №8. с. 1058-1064.
28. Овчинников Ю.А. // Биоорганическая химия. 1978. т.12. №2. с. 205.
29. A.V. Azhayer, A.M. Ozols, A.S. Bushnev, N.B. Dyatkina, S.V. Kochetkova, L.S. Victorova, M.K. Kunhanova, A.A. Krayevsky and B.P. Ejottikh // Nucleic Acids Research. 1979. т.6. №2. с. 625-643.
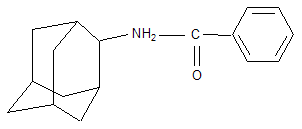 (I)
(I)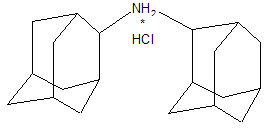 (II)
(II)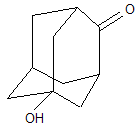 (III)
(III)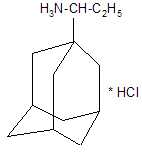 (IV)
(IV)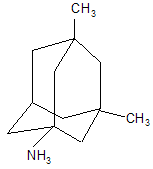 (V)
(V)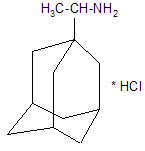 (VI)
(VI)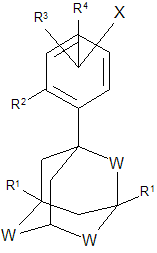
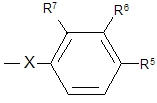 (Q)
(Q) (Q1)
(Q1) (Q2)
(Q2)