
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
Психология и педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Рефераты по сексологии
Рефераты по информатике программированию
Краткое содержание произведений
Реферат: Производство Алюминия
Реферат: Производство Алюминия
Одна весьма сомнительная легенда рассказывает, что однажды к римскому императору Тиберию (42 г. до н. э. — 37 г. н. э.) пришел человек с металлической, небьющейся чашей. Материал чаши якобы был получен из глинозема (Al2O3) и, следовательно, должен был представлять собой алюминий. Опасаясь, что такой металл из глины может обесценить золото и серебро, Тиберий на всякий случай приказал отрубить человеку голову. Разумеется, этому рассказу трудно поверить: самородный алюминий в природе не встречается, а во времена Римской империи не могло быть технических средств, которые позволили бы извлечь алюминий из его соединений.
По распространенности в природе алюминий занимает первое место среди металлов; его содержание в земной коре составляет 7,45%. Однако, несмотря на широкую распространенность в природе, алюминий до конца XIX века принадлежал к числу редких металлов. В чистом виде алюминий не встречается вследствие своей высокой химической активности. Он преимущественно встречается в виде соединений с кислородом и кремнием – алюмосиликатов.
Рудами алюминия могут служить лишь породы, богатые глиноземом (Al2O3) и залегающие крупными массами на поверхности земли. К таким породам относятся бокситы, нефелины — (Na, K)2OּAl2O3ּ2SiO2, алуниты — (Na, K)2SO4ּAl2(SO4)3ּ4Al(OH)3 и каолины (глины), полевой шпат (ортоклаз) — K2OּAl2O3ּ6SiO2.
Основной рудой для получения алюминия являются бокситы. Алюминий в них содержится в виде гидроокисей Al(OH), AlOOH, корунда Al2O3 и каолинита Al2O3ּ2SiO2ּ2H2O. Химический состав бокситов сложен: 28-70% глинозема; 0,5-20% кремнезема; 2-50% окиси железа; 0,1-10% окиси титана. В последнее время в качестве руды стали применять нефелины и алуниты.
Крупные месторождения бокситов находятся на Урале, в Тихвинском районе Ленинградской области, в Алтайском и Красноярском краях.
Нефелин (KּNa2OּAl2O3ּ2SiO2) входит в состав апатитонефелиновых пород (на Кольском полуострове).
Впервые в свободном виде алюминий был выделен в 1825 г. датским физиком Эрстедом путем воздействия амальгамы калия на хлорид алюминия. В 1827г. немецкий химик Велер усовершенствовал способ Эрстеда, заменив амальгаму калия металлическим калием:
AlCl3 + 3K→3KCl + Al (Реакция протекает с выделением тепла).
В 1854 г. Сент-Клер Девиль во Франции впервые применил способ Велера для промышленного производства алюминия, использовав вместо калия более дешевый натрий, а вместо гигроскопичного хлорида алюминия — более стойкий двойной хлорид алюминия и натрия. В 1865 г. русский физико-химик Н. Н. Бекетов показал возможность вытеснения алюминия магнием из расплавленного криолита. Эта реакция в 1888 г. была использована для производства алюминия на первом немецком заводе в Гмелингене. Производство алюминия этими так называемыми «химическими» способами осуществлялось с 1854 г. по 1890 г. В течение 35 лет с помощью этих способов, было получено в общей сложности около 20 т алюминия.
В конце 80-х годов позапрошлого столетия химические способы вытеснил электролитический способ, который позволил резко снизить стоимость алюминия и создал предпосылки к быстрому развитию алюминиевой промышленности. Основоположники современного электролитического способа производства алюминия Эру во Франции и Холл в США независимо друг от друга подали в 1886 г. почти аналогичные заявки на патентование способа получения алюминия электролизом глинозема, растворенного в расплавленном криолите. С момента появления патентов Эру и Холла и начинается современная алюминиевая промышленность, которая более чем за 115 лет своего существования выросла в одну из крупнейших отраслей металлургии.
Технологический процесс получения алюминия состоит из трех основных стадий:
1). Получение глинозема (Al2O3) из алюминиевых руд;
2). Получение алюминия из глинозема;
3). Рафинирование алюминия.
Получение глинозема из руд.
 Глинозем
получают тремя способами: щелочным, кислотным и электролитическим. Наибольшее
распространение имеет щелочной способ (метод К. И. Байера, разработанный в
России в конце позапрошлого столетия и применяемый для переработки
высокосортных бокситов с небольшим количеством (до 5-6%) кремнезема). С тех пор
техническое выполнение его было существенно улучшено. Схема производства
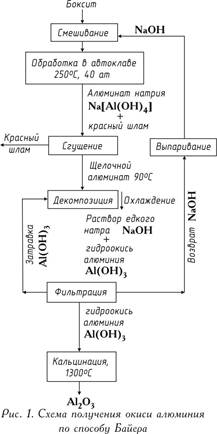
глинозема по способу Байера представлена на рис. 1.
Глинозем
получают тремя способами: щелочным, кислотным и электролитическим. Наибольшее
распространение имеет щелочной способ (метод К. И. Байера, разработанный в
России в конце позапрошлого столетия и применяемый для переработки
высокосортных бокситов с небольшим количеством (до 5-6%) кремнезема). С тех пор
техническое выполнение его было существенно улучшено. Схема производства
глинозема по способу Байера представлена на рис. 1.
Сущность способа состоит в том, что алюминиевые растворы быстро разлагаются при введении в них гидроокиси алюминия, а оставшийся от разложения раствор после его выпаривания в условиях интенсивного перемешивания при 169-170оС может вновь растворять глинозем, содержащийся в бокситах. Этот способ состоит из следующих основных операций:
1). Подготовки боксита, заключающийся в его дроблении и измельчении в мельницах; в мельницы подают боксит, едкую щелочь и небольшое количество извести, которое улучшает выделение Al2O3; полученную пульпу подают на выщелачивание;
2). Выщелачивания боксита (в последнее время применяемые до сих пор блоки автоклав круглой формы частично заменены трубчатыми автоклавами, в которых при температурах 230-250°С (500-520 К) происходит выщелачивание), заключающегося в химическом его разложении от взаимодействия с водным раствором щелочи; гидраты окиси алюминия при взаимодействии со щелочью переходят в раствор в виде алюмината натрия:
AlOOH+NaOH→NaAlO2+H2O
или
Al(OH)3+NaOH→NaAlO2+2H2O;
содержащийся в боксите кремнезем взаимодействует со щелочью и переходит в раствор в виде силиката натрия:
SiO2+2NaOH→Na2SiO3+H2O;
в растворе алюминат натрия и силикат натрия образуют нерастворимый натриевый алюмосиликат; в нерастворимый остаток переходят окислы титана и железа, предающие остатку красный цвет; этот остаток называют красным шламом. По окончании растворения полученный алюминат натрия разбавляют водным раствором щелочи при одновременном понижении температуры на 100°С;
3). Отделения алюминатного раствора от красного шлама обычно осуществляемого путем промывки в специальных сгустителях; в результате этого красный шлам оседает, а алюминатный раствор сливают и затем фильтруют (осветляют). В ограниченных количествах шлам находит применение, например, как добавка к цементу. В зависимости от сорта бокситов на 1 т полученной окиси алюминия приходится 0,6-1,0 т красного шлама (сухого остатка);
4). Разложения алюминатного раствора. Его фильтруют и перекачивают в большие емкости с мешалками (декомпозеры). Из пересыщенного раствора при охлаждении на 60°С (330 К) и постоянном перемешивании извлекается гидроокись алюминия Al(OH)3. Так как этот процесс протекает медленно и неравномерно, а формирование и рост кристаллов гидроокиси алюминия имеют большое значение при ее дальнейшей обработке, в декомпозеры добавляют большое количество твердой гидроокиси — затравки:
Na2OּAl2O3+4H2O→Al(OH)3+2NaOH;
5). Выделения гидроокиси алюминия и ее классификации; это происходит в гидроциклонах и вакуум-фильтрах, где от алюминатного раствора выделяют осадок, содержащий 50-60% частиц Al(OH). Значительную часть гидроокиси возвращают в процесс декомпозиции как затравочный материал, которая и остается в обороте в неизменных количествах. Остаток после промывки водой идет на кальцинацию; фильтрат также возвращается в оборот (после концентрации в выпарных аппаратах — для выщелачивания новых бокситов);
6). Обезвоживания гидроокиси алюминия (кальцинации); это завершающая операция производства глинозема; ее осуществляют в трубчатых вращающихся печах, а в последнее время также в печах с турбулентным движением материала при температуре 1150-1300оС; сырая гидроокись алюминия, проходя через вращающуюся печь, высушивается и обезвоживается; при нагреве происходят последовательно следующие структурные превращения:
|
Al(OH)3→AlOOH→ γ-Al2O3→ α-Al2O3 |
|||
|
200 оС– |
950 оС– |
1200 оС. |
|
В окончательно прокаленном глиноземе содержится 30-50% α-Al2O3 (корунд), остальное γ-Al2O3.
Этим способом извлекается 85-87% от всего получаемого глинозема. Полученная окись алюминия представляет собой прочное химическое соединение с температурой плавления 2050 оС.
Получение алюминия из его окиси
Электролиз окиси алюминия
 Электролитическое
восстановление окиси алюминия, растворенной в расплаве на основе криолита,
осуществляется при 950-970°С в электролизере. Электролизер состоит из
футерованной углеродистыми блоками ванны, к подине которой подводится
электрический ток. Выделившийся на подине, служащей катодом, жидкий алюминий
тяжелее расплава соли электролита, поэтому собирается на угольном основании,
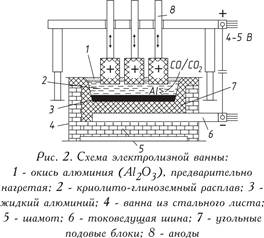
откуда его периодически откачивают (рис. 2). Сверху в электролит погружены
угольные аноды, которые сгорают в атмосфере выделяющегося из окиси алюминия
кислорода, выделяя окись углерода (CO) или двуокись
углерода (CO2). На практике находят применение два типа анодов:
Электролитическое
восстановление окиси алюминия, растворенной в расплаве на основе криолита,
осуществляется при 950-970°С в электролизере. Электролизер состоит из
футерованной углеродистыми блоками ванны, к подине которой подводится
электрический ток. Выделившийся на подине, служащей катодом, жидкий алюминий
тяжелее расплава соли электролита, поэтому собирается на угольном основании,
откуда его периодически откачивают (рис. 2). Сверху в электролит погружены
угольные аноды, которые сгорают в атмосфере выделяющегося из окиси алюминия
кислорода, выделяя окись углерода (CO) или двуокись
углерода (CO2). На практике находят применение два типа анодов:
а) самообжигающиеся аноды Зедерберга, состоящие из брикетов, так называемых «хлебов» массы Зедерберга (малозольный уголь с 25-35% каменноугольного пека), набитых в алюминиевую оболочку; под действием высокой температуры анодная масса обжигается (спекается);
б) обожженные, или «непрерывные», аноды из больших угольных блоков (например, 1900×600×500 мм массой около 1,1 т).
Сила тока на электролизерах составляет 150 000 А. Они включаются в сеть последовательно, т. е. получается система (серия) — длинный ряд электролизеров.
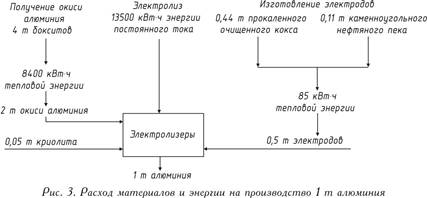
Рабочее напряжение на ванне, составляющее 4-5 В, значительно выше напряжения, при котором происходит разложение окиси алюминия, поскольку в процессе работы неизбежны потери напряжения в различных частях системы. Баланс сырья и энергии при получении 1 т алюминия представлен на рис. 3.
Электролиз хлорида алюминия (метод фирмы Алкоа)
 В реакционном
сосуде окись алюминия превращается сначала в хлорид алюминия. Затем в плотно
изолированной ванне происходит электролиз AlCl3,
растворенного в расплаве солей KCl, NaCl.
Выделяющийся при этом хлор отсасывается и подается для вторичного
использования; алюминий осаждается на катоде.
В реакционном
сосуде окись алюминия превращается сначала в хлорид алюминия. Затем в плотно
изолированной ванне происходит электролиз AlCl3,
растворенного в расплаве солей KCl, NaCl.
Выделяющийся при этом хлор отсасывается и подается для вторичного
использования; алюминий осаждается на катоде.
Преимуществами данного метода перед существующим электролизом жидкого криолитоглиноземного расплава (Al2O3, растворенная в криолите Na3AlF6) считают: экономию до 30% энергии; возможность применения окиси алюминия, которая не годится для традиционного электролиза (например, Al2O3 с высоким содержанием кремния); замену дорогостоящего криолита более дешевыми солями; исчезновение опасности выделения фтора.
Восстановление хлорида алюминия марганцем (Toth — метод)
 При
восстановлении марганцем из хлорида алюминия освобождается алюминий.
Посредством управляемой конденсации из потока хлорида марганца выделяются
связанные с хлором загрязнения. При освобождении хлора хлорид марганца
окисляется в окись марганца, которая затем восстанавливается до марганца,
пригодного к вторичному применению. Сведения в имеющихся публикациях весьма
неточны, так что в данном случае придется отказаться от оценки метода.
При
восстановлении марганцем из хлорида алюминия освобождается алюминий.
Посредством управляемой конденсации из потока хлорида марганца выделяются
связанные с хлором загрязнения. При освобождении хлора хлорид марганца
окисляется в окись марганца, которая затем восстанавливается до марганца,
пригодного к вторичному применению. Сведения в имеющихся публикациях весьма
неточны, так что в данном случае придется отказаться от оценки метода.
Получение рафинированного алюминия
Для алюминия рафинирующий электролиз с разложением водных солевых растворов невозможен. Поскольку для некоторых целей степень очистки промышленного алюминия (Al 99,5 — Al 99,8), полученного электролизом криолитоглиноземного расплава, недостаточна, то из промышленного алюминия или отходов металла путем рафинирования получают еще более чистый алюминий (Al 99, 99 R). Наиболее известен метод рафинирования — трехслойный электролиз.
Рафинирование методом трехслойного электролиза
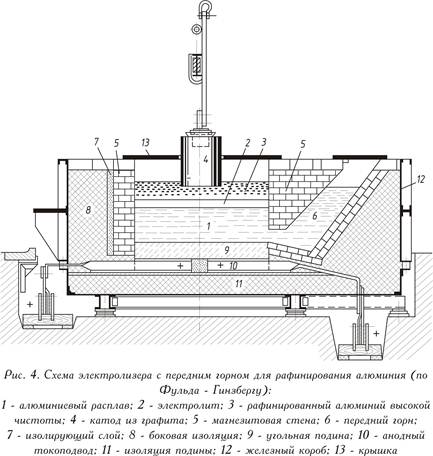
Одетая стальным листом, работающая на постоянном токе (представленная на рис. 4 — см. выше) ванна для рафинирования состоит из угольной подины с токоподводами и теплоизолирующей магнезитовой футеровки. В противоположность электролизу криолитоглиноземного расплава анодом здесь служит, как правило, расплавленный рафинируемый металл (нижний анодный слой). Электролит составляется из чистых фторидов или смеси хлорида бария и фторидов алюминия и натрия (средний слой). Алюминий, растворяющийся из анодного слоя в электролите, выделяется над электролитом (верхний катодный слой). Чистый металл служит катодом. Подвод тока к катодному слою осуществляется графитовым электродом.
Ванна работает при 750-800°С, расход электроэнергии составляет 20 кВтּч на 1 кг чистого алюминия, т. е. несколько выше, чем при обычном электролизе алюминия.
Металл анода содержит 25-35% Cu; 7-12% Zn; 6-9% Si; до 5% Fe и незначительное количество марганца, никеля, свинца и олова, остальное (40-55%) — алюминий. Все тяжелые металлы и кремний при рафинировании остаются в анодном слое. Наличие магния в электролите приводит к нежелательным изменениям состава электролита или к сильному его ошлакованию. Для очистки от магния шлаки, содержащие магний, обрабатывают флюсами или газообразным хлором.
В результате рафинирования получают чистый алюминий (99,99%) и продукты сегрегации (зайгер-продукт), которые содержат тяжелые металлы и кремний и выделяются в виде щелочного раствора и кристаллического остатка. Щелочной раствор является отходом, а твердый остаток применяется для раскисления.
Рафинированный алюминий имеет обычно следующий состав, %: Fe 0,0005-0,002; Si 0,002-0,005; Cu 0,0005-0,002; Zn 0,0005-0,002; Mg следы; Al остальное.
Рафинированный алюминий перерабатывают в полуфабрикат в указанном составе или легируют магнием (см. табл. 1.2.).
ТАБЛИЦА 1.2. Химический состав алюминия повышенной чистоты и первичного алюминия по DIN 17122, лист 1.
|
Марка |
Номер |
Допустимые примеси* , % |
|||||||
|
всего |
в том числе |
||||||||
|
Si |
Fe |
Ti |
Cu |
Zn |
прочие |
||||
| A199,99R | 3.0400 | 0,01 | 0,006 | 0,005 | 0,002 | 0,003 | 0,005 | 0,001 | |
| A199,9H | 3.0300 | 0,1 | 0,050 | 0,035 | 0,006 | 0,005 | 0,04 | 0,003 | |
| A199,8H | 3.0280 | 0,2 | 0,15 | 0,15 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199,7H | 3.0270 | 0,3 | 0,20 | 0,25 | 0,03 | 0,01 | 0,06 | 0,01 | |
| A199,5H** | 3.0250 | 0,5 | 0,30 | 0,40 | 0,03 | 0,02 | 0,07 | 0,03 | |
| A199H | 3.0200 | 1,0 | 0,5 | 0,6 | 0,03 | 0,02 | 0,08 | 0,03 | |
|
* Насколько возможно определить обычными методами исследования. ** Чистый алюминий для электротехники (алюминиевые проводники) поставляют в виде первичного алюминий 99,5, содержащего не более 0,03% (Ti + Cr + V + Mn); обозначается в этом случае E-A1, номер материала 3.0256. В остальном соответствует нормам VDE-0202. |
|||||||||
Рафинирование путем алюмоорганических комплексных соединений и зонной плавкой
Алюминий степени чистоты выше марки A1 99,99 R может быть получен рафинирующим электролизом чистого или технически чистого алюминия с применением в качестве электролита комплексных алюмоорганических соединений алюминия. Электролиз проходит при температуре около 1000°С между твердыми алюминиевыми электродами и в принципе схож с рафинирующим электролизом меди. Природа электролита диктует необходимость работать без доступа воздуха и при низкой плотности тока.
Этот вид рафинирующего электролиза, применяемым сначала лишь в лабораторном масштабе, уже осуществляется в небольшом производственном масштабе — изготовляется несколько тонн металла в год. Номинальная степень очистки получаемого металла 99,999-99,9999%. Потенциальными областями применения металла такой чистоты являются криогенная электротехника и электроника.
Возможно применение рассмотренного метода рафинирования и в гальванотехнике.
Еще более высокую чистоту — номинально до A1 99,99999 — можно получить последующей зонной плавкой металла. При переработке алюминия повышенной чистоты в полуфабрикат, лист или проволоку необходимо, учитывая низкую температуру рекристаллизации металла, принимать особые меры предосторожности. Примечательным свойством рафинированного металла является его высокая электропроводность в области криогенных температур.
Получение вторичного алюминия
Переработка вторичного сырья и отходов производства является экономически выгодной. Получаемыми при этом вторичными сплавами удовлетворяется около 25% общей потребности в алюминии.
 Важнейшей
областью применения вторичных сплавов является производство алюминиевого
фасонного литья. В DIN 1725, лист 2 наряду со
стандартными марками сплавов приведены многочисленные марки сплавов,
производимых литейными заводами. Перечень сплавов, выпускаемых этими заводами,
содержит, кроме стандартных, некоторые нестандартные сплавы.
Важнейшей
областью применения вторичных сплавов является производство алюминиевого
фасонного литья. В DIN 1725, лист 2 наряду со
стандартными марками сплавов приведены многочисленные марки сплавов,
производимых литейными заводами. Перечень сплавов, выпускаемых этими заводами,
содержит, кроме стандартных, некоторые нестандартные сплавы.
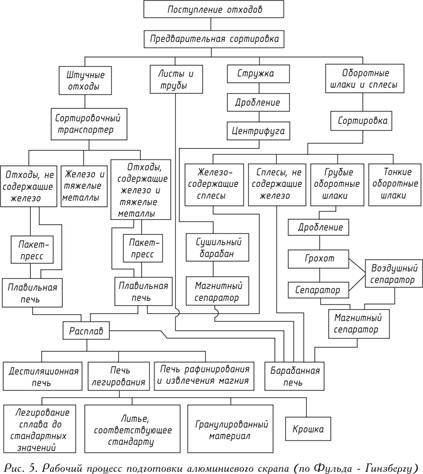
Безупречное приготовление алюминиевого скрапа в самых разнообразных пропорциях можно осуществлять только на специально оборудованных плавильных заводах. Представление о сложном рабочем процессе на таком заводе дает рис. 5.
Отходы переплавляют после грубой предварительной сортировки. Содержащиеся в этих отходах железо, никель или медь, точка плавления которых выше точки плавления алюминия, при плавке в плавильной пороговой печи остаются в ней, а алюминий выплавляется. Для удаления из отходов неметаллических включений типа окислов, нитридов, карбидов или газов применяют обработку расплавленного металла солями или (что рациональней) продувку газом — хлором или азотом.
Для удаления металлических примесей из расплава известны различные методы, например присадка магния и вакуумирование — метод Бекша (Becksche); присадка цинка или ртути с последующим вакуумированием — субгалогенный метод. Удаление магния ограничивается введением в расплавленный металл хлора. Путем введения добавок, точно определяемых составом расплава, получают заданный литейный сплав.
Производство алюминия технической чистоты
Электролитический способ — единственный применяющийся во всем мире для производства металлического алюминия технической чистоты. Все другие способы (цинкотермический, карбидотермический, субхлоридный, нитридный и др.), с помощью которых алюминий может быть извлечен из алюминиевых руд, разрабатывались в лабораторном и опытно-промышленных масштабах, однако пока не нашли практического применения.
Для получения алюминиево-кремниевых сплавов успешно применяется электротермический способ, впервые разработанный и осуществленный в промышленном масштабе в СССР. Он состоит из двух стадий: на первой стадии получают первичный алюминиево-кремниевый сплав с содержанием 60-63 % Al путем прямого восстановления алюмо-кремнистых руд в рудно-термических электрических печах; на второй стадии первичный сплав разбавляют техническим алюминием, получая силумин и другие литейные и деформируемые алюминиево-кремниевые сплавы. Ведутся исследования по извлечению из первичного сплава алюминия технической чистоты.
В целом получение алюминия электролитическим способом включает в себя производство глинозема (окиси алюминия) из алюминиевых руд, производство фтористых солей (криолита, фтористого алюминия и фтористого натрия), производство углеродистой анодной массы, обожженных угольных анодных и катодных блоков и других футеровочных материалов, а также собственно электролитическое производство алюминия, которое является завершающим этапом современной металлургии алюминия.
Характерным для производства глинозема, фтористых солей и углеродистых изделий является требование максимальной степени чистоты этих материалов, так как в криолитоглиноземных расплавах, подвергающихся электролизу, не должны содержаться примеси элементов, более электроположительных, чем алюминий, которые, выделяясь на катоде в первую очередь, загрязняли бы металл.
В глиноземе марок Г-00, Г-0 и Г-1, которые преимущественно используются при электролизе, содержание SiO2 составляет 0,02-0,05%, a Fe2O3 — 0,03-0,05%. В криолите в среднем содержится 0,36-0,38% SiO2 и 0,05-0,06% Fe2O3, во фтористом алюминии 0,30-0,35% (SiO2 + Fe2O3). В анодной массе содержится не более 0,25% SiO2 и 0,20% Fe2O3.
Важнейшая алюминиевая руда, из которой извлекают глинозем, боксит. В боксите алюминий присутствует в форме гидроокиси алюминия. В Советском Союзе, кроме боксита, для получения глинозема применяют нефелиновую породу — алюмосиликат натрия и калия, а также алунитовую породу, в которой алюминий находится в виде его сульфата. Сырьем для изготовления анодной массы и обожженных анодных блоков служат углеродистые чистые материалы — нефтяной или пековый кокс и каменноугольный пек в качестве связующего, а для производства криолита и других фтористых солей — фтористый кальций (плавиковый шпат).
При электролитическом получении алюминия глинозема Al2O3, растворенный в расплавленном криолите Na3AlF6, электрохимически разлагается с разрядом катионов алюминия на катоде (жидком алюминии), а кислородсодержащих ионов (ионов кислорода) — на углеродистом аноде.
По современным представлениям, криолит в
расплавленном состоянии диссоциирует на ионы ![]() и
и ![]() :
: ![]() , а глинозем — на
комплексные ионы
, а глинозем — на
комплексные ионы ![]() и
и ![]() :
: ![]() , которые находятся в
равновесии с простыми ионами:
, которые находятся в
равновесии с простыми ионами: ![]() ,
, ![]() .
.
Основным процессом, происходящим на катоде, является восстановление ионов трехвалентного алюминия: Al3+ + 3e → Al (I).
Наряду с основным процессом возможен неполный разряд трехвалентных ионов алюминия с образованием одновалентных ионов: Al3+ + 2e → Al+ (II) и, наконец, разряд одновалентных ионов с выделением металла: Al+ + e → Al (III).
При определенных условиях (относительно большая концентрация ионов Na+, высокая температура и др.) может происходить разряд ионов натрия с выделением металла: Na+ + e → Na (IV). Реакции (II) и (IV) обусловливают снижение выхода алюминия по току.
На угольном аноде происходит разряд ионов кислорода: 2O2– – 4e → O2. Однако кислород не выделяется в свободном виде, так как он окисляет углерод анода с образованием смеси CO2 и CO.
Суммарная реакция, происходящая в электролизере, может быть представлена уравнением Al2O3 + xC ↔ 2Al + (2x–3)CO + (3–x)CO2.
В состав электролита промышленных алюминиевых электролизеров, помимо основных компонентов — криолита, фтористого алюминия и глинозема, входят небольшие количества (в сумме до 8-9%) некоторых других солей — CaF2, MgF2, NaCl и LiF (добавки), которые улучшают некоторые физико-химические свойства электролита и тем самым повышают эффективность работы электролизеров. Максимальное содержание глинозема в электролите составляет обычно 6-8%, снижаясь в процессе электролиза. По мере обеднения электролита глиноземом в него вводят очередную порцию глинозема. Для нормальной работы алюминиевых электролизеров отношение NaF: AlF3 в электролите поддерживают в пределах 2,7-2,8, добавляя порции криолита и фтористого алюминия.
В производстве алюминия применяют электролизеры с самообжигающимися угольными анодами и боковым или верхним подводом тока, а также электролизеры с предварительно обожженными угольными анодами. Наиболее перспективна конструкция электролизеров с обожженными анодами, позволяющая увеличить единичную мощность агрегата, снизить удельный расход электроэнергии постоянного тока на электролиз, получить более чистый металл, улучшить санитарно-гигиенические условия труда и уменьшить выбросы вредных веществ в атмосферу.
Основные технические параметры и показатели работы алюминиевых электролизеров различного типа приведены в табл. 1.3.
ТАБЛИЦА 1.3
ОСНОВНЫЕ ТЕХНИЧЕСКИЕ ПАРАМЕТРЫ И ПОКАЗАТЕЛИ РАБОТЫ АЛЮМИНИЕВЫХ ЭЛЕКТРОЛИЗЕРОВ
|
Параметры и показатели |
С самообжигающимися анодами |
С обожженными анодами |
|
|
боковой токоподвод |
верхний токоподвод |
||
| Сила тока, кА | 60—120 | 60—155 | 160—255 |
| Суточная производительность электролизера, т | 0,42—0,85 | 0,40—1,10 | 1,10—1,74 |
|
Анодная плотность тока, А/см2 |
0,80—0,90 | 0,65—0,70 | 0,70—0,89 |
| Среднее напряжение на электролизере, В | 4,45—4,65 | 4,50—4,70 | 4,30—4,50 |
| Выход по току, % | 85—88 | 84—86 | 85—89 |
| Расходные коэффициенты на 1 т алюминия: | |||
| электроэнергии постоянного тока, кВтּч | 15100—16200 | 15500—17300 | 14500—15500 |
| глинозема, кг | 1920—1940 | 1920—1940 | 1920—1940 |
| анодной массы, кг | 520—560 | 560—620 | — |
| обожженных анодов, кг | — | — | 540—600 |
| Фтористых солей в пересчете на фтор, кг | 20—30 | 25—35 | 15—25 |
Первичный алюминий, извлекаемый из электролизеров (алюминий-сырец), содержит ряд примесей, которые можно подразделить на три группы: неметаллические (фтористые соли, α- и γ-глинозем, карбид и нитрид алюминия, угольные частицы, механически увлекаемые при выливке металла из электролизера); металлические (железо, кремний), переходящие из сырья, угольных материалов и конструктивных элементов электролизера; газообразные — преимущественно водород, который образуется в металле в результате электролитического разложения воды, попадающей в электролит с сырьем.
Из металлических примесей, помимо железа и кремния, содержится наибольшее количество галлия, цинка, титана, марганца, натрия, ванадия, хрома, меди. Содержание этих и некоторых других металлических микропримесей в электролитическом алюминии приведено ниже, %:
|
Элемент |
V |
Mn |
Cr |
Ti |
Cu |
Zn |
| Среднее содержание | 0,0025 | 0,003 | 0,0025 | 0,004 | 0,002 | 0,007 |
| Пределы изменения | 0,001—0,008 | 0,001—0,006 | 0,001—0,008 | 0,002—0,008 | 0,001—0,008 | 0,002—0,014 |
|
Элемент |
Ni |
Li |
P |
S |
Ga |
Na |
| Среднее содержание | <0,002 | 0,0002 | 0,001 | 0,0005 | 0,008 | 0,004 |
| Пределы изменения | <0,001—0,004 | 0,0001—0,0003 | 0,001—0,0024 | 0,0001—0,0009 | 0,004—0,012 | 0,002—0,008 |
Основным источником поступления металлических микропримесей в алюминий является глинозем, который в зависимости от вида исходного сырья может содержать галлий, цинк, калий, фосфор, серу, ванадий, титан и хром. Углеродистые материалы (анодная масса, обожженные аноды, катодные изделия) служат источником таких микропримесей, как, например, ванадий, титан, марганец, цинк.
Электролизом криолито-глиноземных расплавов при условии применения чистых исходных материалов (в первую очередь глинозема и углеродистых материалов) удается получить алюминий-сырец марок А85 и А8 (99,85 и 99,80%). Наибольшая доля металла этих марок (60-70 % от общего выпуска) получается на электролизерах с обожженными анодами, а также на электролизерах с боковым подводом тока (до 70 % от общего производства). На электролизерах с самообжигающимися анодами и верхним токоподводом выпуск алюминия-сырца марки А8 невысок (составляет 1-3%), а металл марки А85 получить не удается из-за значительных примесей железа, поступающего в алюминий из несырьевых источников (анодные штыри, чугунные секции газосборников, технологический инструмент, катодный узел).
Расплавленный первичный алюминий, извлеченный из электролизеров с помощью вакуумного ковша, поступает в литейное отделение для рафинирования от неметаллических и газовых примесей и дальнейшей переработки в товарную продукцию (чушки, цилиндрические и плоские слитки, катанку и т. п.). Перед разливкой алюминий-сырец выдерживают в расплавленном состоянии в электрических печах сопротивления (миксерах) или в газовых отражательных печах. В этих печах не только проводят рациональную шихтовку различных по составу порций жидкого алюминия, но и частично очищают от неметаллических включений, окисных пленок и натрия.
Разливка алюминия из миксера в чушки производится с помощью литейных машин конвейерного типа; цилиндрические и плоские слитки изготавливают методом полунепрерывного литья, а для получения катанки применяют специальные агрегаты совмещенного литья и прокатки.
На отечественных алюминиевых заводах при литье слитков алюминий, поступающий из миксера в кристаллизатор литейной машины, подвергают простейшему виду рафинирования — фильтрации расплава через стеклосетку с ячейками размером от 0,6×0,6 до 1,7×1,7 мм. Этот метод позволяет очищать алюминий только от очень грубых окисных включений; более совершенен метод фильтрации расплава через стеклосетку в восходящем потоке. При таком способе фильтрования частицы окисных включений, сталкиваясь с сеткой, не захватываются потоком расплава, а осаждаются на дне литейного желоба.
Для одновременной очистки алюминия, как от неметаллических примесей, так и от водорода успешно применяется метод фильтрации через флюсовый фильтр в сочетании с продувкой азотом. В качестве флюса можно использовать кислый электролит алюминиевых электролизеров. В результате такой очистки содержание водорода в алюминии снижается с 0,22 до 0,16 см3 на 100 г металла.
В первичном алюминии, используемом для производства сплавов системы Al—Mg, содержание натрия не должно превышать 0,001 %. Это связано с тем, что присутствие натрия в этих сплавах ухудшает механические и другие эксплуатационные свойства изделий, применяемых в ряде отраслей народного хозяйства.
Наиболее эффективным методом одновременного рафинирования алюминия от натрия, водорода и неметаллических примесей является продувка расплавленного металла газовой смесью азота с 2-10% хлора, вводимой в расплав в виде мелких пузырей с помощью специальных устройств. Этот способ рафинирования позволяет снизить содержание натрия в алюминии до 0,0003—0,001% при расходе газовой смеси от 0,8 до 1,5 м3/т металла.
Расход электроэнергии на производство 1 т товарного алюминия из металла-сырца при использовании электропечей составляет 150-200 кВтּч; безвозвратные потери металла на литейном переделе равны 1,5-5 % в зависимости от вида товарной продукции.
Получение алюминия высокой чистоты
Для получения алюминия высокой чистоты (марок А995—А95) первичный алюминий технической чистоты электролитически рафинируют. Это позволяет снизить в алюминии содержание металлических и газообразных примесей и тем самым значительно повысить его электропроводность, пластичность, отражательную способность и коррозионную стойкость.
Электролитическое рафинирование алюминия осуществляют электролизом расплавленных солей по трехслойному способу. Сущность способа заключается в следующем. В рафинировочном электролизере имеются три расплавленных слоя. Нижний, наиболее тяжелый, лежит на токопроводящей подине и служит анодом; он называется анодным сплавом и представляет собой сплав рафинируемого алюминия с медью, которую вводят для утяжеления слоя. Средний слой — расплавленный электролит; его плотность меньше плотности анодного сплава и выше плотности чистого рафинированного (катодного) алюминия, находящегося над электролитом (верхний, третий жидкий слой).
При анодном растворении все примеси более электроположительные, чем алюминий (Fe, Si, Ti, Cu и др.), остаются в анодном сплаве, не переходя в электролит. Анодно растворяться будет только алюминий, который в форме ионов Al3+ переходит в электролит: Al – 3e → Al3+.
При электролизе ионы алюминия переносятся к катоду, на котором и разряжаются: Al3+ + 3e → Al. В результате на катоде накапливается слой расплавленного рафинированного алюминия.
Если в анодном сплаве присутствуют примеси более электроотрицательные, чем алюминий (например, Ba, Na, Mg, Ca), то они могут электрохимически растворяться на аноде вместе с алюминием и в виде ионов переходить в электролит. Поскольку содержание электроотрицательных примесей в алюминии-сырце невелико, в заметном количестве в электролите они не накапливаются. Разряда этих ионов на катоде практически не происходит, так как их электродный потенциал электроотрицательнее алюминия.
В качестве электролита при электролитическом рафинировании алюминия в Советском Союзе и в большинстве стран применяют фторидно-хлоридный электролит, состав которого 55-60% BaCl2, 35-40% AlF4+NaF и 0-4% NaCl. Молярное отношение NaF : AlF3 поддерживают 1,5-2,0; температура плавления электролита 720-730°C; температура процесса электролиза около 800°C; плотность электролита 2,7 г/см3.
Анодный сплав готовят из первичного алюминия и чистой меди (99,90-99,95% Cu), которую вводят в металл в количестве 30-40%. Плотность жидкого анодного сплава такого состава 3-3,5 г/см3; плотность же чистого расплавленного катодного алюминия равна 2,3 г/см3. При таком соотношении плотностей создаются условия, необходимые для хорошего разделения трех расплавленных слоев.
В четверной системе Al—Cu—Fe—Si, к которой относится анодный сплав, образуется эвтектика с температурой плавления 520°C. Охлаждая анодный сплав, содержащий примеси железа и кремния в количествах выше эвтектических концентраций, можно выделить железо и кремний в твердую фазу в виде интерметаллических соединений FeSiAl5 и Cu2FeAl7. Так как температура анодного сплава в карманах электролизера на 30-40°C ниже температуры анодного сплава в рабочем пространстве ванны, в них (по мере накопления в анодном сплаве железа и кремния) будут выделяться твердые интерметаллические осадки. Периодически удаляя эти осадки, очищают анодный сплав (без его обновления) от примесей железа и кремния. Так как в анодном сплаве концентрируется галлий, то извлекаемые из электролизера осадки (30-40 кг на 1 т алюминия) могут служить источником получения этого металла.
Для электролитического рафинирования служат электролизеры, которые по конструкции напоминают электролизеры с обожженными анодами для электролитического получения первичного алюминия, но имеют другое подключение полюсов: подина служит анодом, а верхний ряд электродов — катодом. Современные электролизеры для электролитического рафинирования алюминия рассчитаны на силу тока до 75 кА.
Ниже приведены основные технико-экономические показатели электролизеров за 1979 г., достигнутые отечественными (1, 2, 3) предприятиями.
Электрохимический выход по току, рассчитанный по вылитому из электролизера металлу, составляет 97-98%. Фактический же выход по току, рассчитанный по количеству товарного металла, составляет 92-96%.
Сила тока, кА |
23,5 | 62,9 | 69,8* |
|
Среднее напряжение, В |
5,43 | 5,68 | 5,69 |
|
Выход по току, % |
95,7 | 93,0 | 92,7 |
|
Расход электроэнергии постоянного тока, кВтּч/т |
17 370 | 18 700 | 19 830 |
|
Суммарный электроэнергии переменного тока, кВтּч/т |
18 670 | 19 590 | 20 780 |
Уровни, см |
|||
|
катодного алюминия |
16,6 | 12,9 | 14,6 |
|
электролита |
13,3 | 11,6 | 14,2 |
|
анодного сплава |
40,1 | 29,5 | 30,0 |
|
Расходные коэффициенты, кг/т: |
|||
|
хлористый барий |
40,5 | 41,5 | 27,0 |
|
криолит |
27,7 | 21,0 | 16,5 |
|
фтористый алюминий |
6,7 | 13,1 | 3,8 |
|
хлористый натрий |
1,0 | 4,8 | — |
|
алюминий-сырец |
1020 | 1028 | 1032 |
|
графит |
11,9 | 11,5 | 16,6 |
|
медь |
9,8 | 15,5 | 16,4 |
|
Выпуск алюминия высокой чистоты, % марок: |
|||
|
А995 |
47,8** | 3,5 | 2,1 |
|
А99 |
30,4 | 67,1 | 54,2 |
|
А97 |
8,3 | 21,5 | 43,7 |
|
А95 |
10,4 | 7,9 | — |
|
ниже А95 |
3,1 | — | — |
|
* Показатели производства алюминия высокой чистоты. ** Сортность по электролизерам без расшихтовки. |
|||
Основным фактором, снижающим выход по току, помимо прямых потерь тока на разряд более электроотрицательных ионов, потерь металла за счет его окисления и механических потерь алюминия, является работа электролизеров с выпуском несортового металла, который вновь возвращается в анодный сплав для последующего рафинирования. Эти периоды работы электролизеров имеют место при пуске электролизеров и нарушениях технологического режима.
Электролитическое рафинирование алюминия является очень энергоемким производством. Расход электроэнергии в переменном токе, включая энергию, затраченную на подготовку электролита и анодного сплава, работу вентиляционных устройств и транспортных средств, а также потери на преобразование переменного тока в постоянный, составляет 18,5-21,0 тыс. кВтּч на 1 т алюминия. Энергетический к. п. д. рафинировочных электролизеров не превышает 5-7%, т. е. 93-95% энергии расходуется в виде потерь тепла, выделяемого в основном в слое электролита (примерно 80-85% от общего прихода тепла). Следовательно, основными путями дальнейшего снижения удельного расхода электроэнергии на электролитическое рафинирование алюминия являются совершенствование теплоизоляции электролизера (особенно верхней части конструкции) и снижение слоя электролита (уменьшение междуэлектродного расстояния).
Чистота алюминия, рафинированного по трехслойному методу, 99,995%; она определяется по разности с пятью основными примесями — железом, кремнием, медью, цинком и титаном. Количество получаемого металла такой марки может составлять 45-48% от общего выпуска (без его расшихтовки с более низкими, сортами).
Следует, однако, отметить, что в электролитически рафинированном алюминии содержатся в меньших количествах примеси других металлов, что снижает абсолютную чистоту такого алюминия. Радиоактивационный анализ позволяет обнаружить в электролитически рафинированном алюминии до 30 примесей, суммарное содержание которых примерно 60ּ10–4%. Следовательно, чистота рафинированного алюминия по разности с этими примесями составляет 99,994%.
Помимо примесей, предусмотренных ГОСТом (см. табл. 1.1), в наиболее распространенной марке (А99) электролитически рафинированного алюминия содержится, %: Cr 0,00016; V 0,0001; Ga 0,0006; Pb 0,002; Sn 0,00005; Ca 0,002-0,003; Na 0,001-0,008; Mn 0,001-0,007; Mg 0,001-0,007; As<0,0001; Sb<0,00002; Bi<0,00001; Cd<0,000001; S 0,0007.
Один из источников загрязнения катодного алюминия — графитовые токоотводы, содержащие окись железа и кремния и постоянно соприкасающиеся с рафинированным алюминием. Если ток к катодному алюминию подводить непосредственно алюминиевыми шинами и применять инструмент из очень чистого графита, можно получать металл чистотой 99,999% по разности с определяемыми примесями (Fe, Si, Cu, Zn и Ti). B таком металле содержится в среднем, %: Si 0,0002; Fe 0,00032; Cu 0,0002; Zn 0,0002 и Ti 0,00005. Однако из-за технических трудностей такой способ подвода тока пока не нашел широкого промышленного применения.
Получение алюминия особой чистоты
Алюминий особой чистоты (марки A999) может быть получен тремя способами: зонной плавкой, дистилляцией через субгалогениды и электролизом алюминий-органических соединений. Из перечисленных способов получения алюминия особой чистоты практическое применение в СССР получил способ зонной плавки.
Принцип зонной плавки заключается в многократном прохождении расплавленной зоны вдоль слитка алюминия. По величине коэффициентов распределения К=Ств/Сж (где Ств — концентрация примеси в твердой и Сж — в жидкой фазе), которые в значительной мере определяют эффективность очистки от примесей, эти примеси могут быть разбиты на три группы. К первой группе относятся примеси, понижающие температуру плавления алюминия; они имеют К<1, при зонной плавке концентрируются в расплавленной зоне и переносятся ею к конечной части слитка. К числу этих примесей принадлежат Ga, Sn, Be, Sb, Ca, Th, Fe, Co, Ni, Ce, Te, Ba, Pt, Au, Bi, Pb, Cd, In, Na, Mg, Cu, Si, Ge, Zn. Ко второй группе принадлежат примеси, повышающие температуру плавления алюминия; они характеризуются К>1 и при зонной плавке концентрируются в твердой (начальной) части слитка. К этим примесям относятся Nb, Ta, Cr, Ti, Mo, V. К третьей группе относятся примеси с коэффициентом распределения, очень близким к единице (Mn, Sc). Эти примеси практически не удаляются при зонной плавке алюминия.
Алюминий, предназначенный для зонной плавки, подвергают некоторой подготовке, которая заключается в фильтрации, дегазации и травлении. Фильтрация необходима для удаления из алюминия тугоплавкой и прочной окисной пленки, диспергированной в металле. Окись алюминия, присутствующая в расплавленном алюминии, может при его затвердевании создавать центры кристаллизации, что ведет к получению поликристаллического слитка и нарушению эффекта перераспределения примесей между твердым металлом и расплавленной зоной. Фильтрацию алюминия ведут в вакууме (остаточное давление 0,1-0,4 Па) через отверстие в дне графитового тигля диаметром 1,5-2 мм. Предварительную дегазацию алюминия перед зонной плавкой (также нагреванием в вакууме) проводят для предупреждения разбрызгивания металла при расплавлении зоны в случае проведения процесса в глубоком вакууме. Последняя стадия подготовки алюминия к зонной плавке — травление его поверхности смесью концентрированных соляной и азотной кислот.
Так как алюминий обладает значительной химической активностью и в качестве основного материала для контейнеров (лодочек) применяют особо чистый графит, то зонную плавку алюминия проводят в вакууме или в атмосфере инертного газа (аргон, гелий).
Зонной плавкой в вакууме обеспечивается большая чистота алюминия вследствие улетучивания части примесей при вакуумировании (магния, цинка, кадмия, щелочных и щелочноземельных металлов), а также исключается загрязнение очищенного металла примесями в результате применения защитных инертных газов. Зонную плавку алюминия в вакууме можно проводить при непрерывной откачке кварцевой трубы, куда помещают графитовую лодочку со слитком алюминия, а также в запаянных кварцевых ампулах, из которых предварительно откачивают воздух до остаточного давления примерно 1ּ10–3 Па.
Для создания расплавленной зоны на слитке алюминия при его зонной плавке может быть применен нагрев с помощью небольших печей сопротивления или же токов высокой частоты. Для электропитания печей электросопротивления не требуется сложной аппаратуры, печи просты в эксплуатации. Единственный недостаток этого метода нагрева — небольшое сечение слитка очищаемого алюминия.
Индукционный нагрев токами высокой частоты — идеальный способ создания расплавленной зоны на слитке при зонной плавке. Метод высокочастотного нагрева (помимо того, что он позволяет осуществить зонную плавку слитков больших сечений) имеет важное преимущество, заключающееся в том, что расплавленный металл непрерывно перемешивается в зоне; это облегчает диффузию атомов примеси от фронта кристаллизации в глубь расплава.
Впервые промышленное производство алюминия высокой чистоты зонной плавкой было освоено на Волховском алюминиевом заводе в 1965 г. на установке УЗПИ-3, разработанной ВАМИ. Эта установка была оснащена четырьмя кварцевыми ретортами с индукционным нагревом, при этом индукторы были подвижными, а контейнеры с металлом неподвижными. Производительность ее составляла 20 кг металла за цикл очистки. Впоследствии была создана и введена в промышленную эксплуатацию в 1972 г. на Волховском алюминиевом заводе более высокопроизводительная цельнометаллическая установка УЗПИ-4.
Эффективность очистки алюминия при зонной плавке может быть охарактеризована следующими данными. Если суммарное содержание примесей в электролитически рафинированном алюминии составляет (30÷60)ּ10–4%, то после зонной плавки оно снижается до (2,8÷3,2)ּ10–4%, т. е. в 15-20 раз. Это отвечает остаточному электросопротивлению алюминия ρ○ (при температуре жидкого гелия 4,2 К) соответственно (20÷40)ּ10–10 и (1,8÷2,1)ּ10–10 или чистоте 99,997—99,994 и 99,9997%. В табл. 1.4 (см. ниже) приведены данные радиоактивационного анализа о содержании некоторых примесей в зонно-очищенном алюминии и электролитически рафинированном. Эти данные свидетельствуют о сильном снижении содержания большинства примесей, хотя такие примеси, как марганец и скандий, при зонной плавке практически не удаляются.
В последние годы в ВАМИ разработана и опробована в промышленных условиях технология получения алюминия чистотой 99,9999% методом каскадной зонной плавки. Сущность способа каскадной зонной плавки заключается в том, что очистку исходного алюминия чистотой А999 ведут, последовательно повторяя циклы (каскады) зонной планки. При этом исходным материалом каждого последующего каскада служит средняя, наиболее чистая часть слитка, получаемого в результате предыдущего цикла очистки.
ТАБЛИЦА 1.4
СОДЕРЖАНИЕ ПРИМЕСЕЙ В ЭЛЕКТРОЛИТИЧЕСКИ РАФИНИРОВАННОМ И ЗОННООЧИЩЕННОМ АЛЮМИНИИ, ×10–4 %
|
Примесь |
Исходный алюминий (электролитически рафинированный 99,993-99,994 %) |
Алюминий после зонной плавки |
|
|
графит, вакуум |
алунд, воздух |
||
| Медь | 1,9 | 0,02 | 0,08 |
| Мышьяк | 0,15 | 0,0015 | 0,001 |
| Сурьма | 1,2 | 0,03 | 0,02 |
| Уран | 0,002 | — | — |
| Железо | 3 | ≤0,2 | ≤0,3 |
| Галий | 0,3 | 0,02 | 0,05 |
| Марганец | 0,2—0,3 | 0,1—0,2 | 0,15 |
| Скандий | 0,4—0,5 | 0,4—0,5 | 0,4—0,5 |
| Иттрий | 0,02—0,04 | <<0,001 | <<0,001 |
| Лютеций | 0,002—0,004 | <<0,0001 | <<0,0001 |
| Гольмий | 0,005—0,01 | <<0,0001 | <<0,0001 |
| Гадолиний | 0,02—0,04 | <<0,01 | <<0,01 |
| Тербий | 0,003—0,006 | <<0,001 | <<0,001 |
| Самарий | 0,05—0,01 | <<0,0001 | <<0,0001 |
| Неодим | 0,1—0,2 | <<0,01 | <<0,01 |
| Празеодим | 0,05—0,1 | <<0,001 | <<0,001 |
| Церий | 0,3—0,6 | <<0,01 | <<0,01 |
| Лантан | 0,01 | <<0,001 | <<0,001 |
| Никель | 2,3 | — | <1 |
| Кадмий | 3,5 | <<0,01 | 0,02—0,07 |
| Цинк | 20 | <<0,05 | 1 |
| Кобальт | 0,01 | <<0,01 | <<0,01 |
| Натрий | 1—2 | <0,2 | <0,2 |
| Калий | 0,05 | 0,01 | 0,01 |
| Барий | 6 | — | — |
| Хлор | 0,01 | <0,01 | <0,01 |
| Фосфор | 3 | 0,04 | — |
| Сера | 15 | 0,5—1,5 | — |
| Углерод | 1—2 | — | 1—2 |
| Примечание. Количества теллура, висмута, серебра, молибдена, хрома, циркония, кальция, стронция, рубидия, церия, индия, селена и ртути в алюминии после зонной плавки ниже чувствительности радиоактивного анализа. | |||
В табл. 1.5 (см. ниже) приведены результаты масс-спектрального анализа и измерения R293 К/R4,2 К алюминия, полученного каскадной зонной плавкой. Из приведенных данных можно сделать заключение, что чистота такого алюминия, определенная по разности с десятью основными примесями (Si, Fe, Mg, Mn, Ti, Cu, Cr, Zn, Na, и V), составляет >99,9999%. Этот вывод косвенно подтверждается величиной R293 К/R4,2 К, которая во всех образцах составляла >30ּ103.
Для получения металла чистотой 99,9999% достаточно провести два каскада зонной плавки (см. табл. 1.5). Дальнейшее увеличение числа каскадов не повышает чистоту алюминия, хотя и увеличивает общий выход металла чистотой 99,9999%.
Другим возможным процессом для получения алюминия особой чистоты является его дистилляция через субгалогениды, в частности через субфторид алюминия.
Давление насыщенных паров металлического алюминия недостаточно высоко, чтобы осуществить его непосредственную дистилляцию с практически приемлемыми скоростями. Однако при нагревании в вакууме (при 1000-1050°С) с AlF3 алюминий образует легколетучий субфторид AlF, который перегоняется в холодную зону (800°С), где вновь распадается (диспропорционирует) с выделением чистого алюминия:
![]()
Возможность глубокой очистки алюминия от примеси в основном обусловлена тем, что вероятность образования субсоединений алюминия значительно больше вероятности образования субсоединений примеси.
ТАБЛИЦА 1.5
РЕЗУЛЬТАТЫ МАСС-СПЕКТРАЛЬНОГО АНАЛИЗА И ИЗМЕРЕНИЙ R293 К/R4,2 К АЛЮМИНИЯ КАСКАДНОЙ ЗОННОЙ ПЛАВКИ. [9]
|
Число каскадов |
|
Содержание примесей, ×10–4 % |
|||||
|
Si |
Fe |
Mg |
Mn |
Ti |
сумма |
||
| Исходный | 18,3 | 0,210 | <0,103 | 0,89 | <0,061 | 0,069 | 1,544 |
| A999 | |||||||
| 2 | 36,5 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 38,0 | <0,062 | <0,103 | 0,006 | <0,061 | 0,017 | 0,460 |
| 2 | 39,5 | 0,073 | <0,103 | 0,045 | <0,061 | 0,07 | 0,563 |
| 3 | 32,0 | 0,204 | <0,103 | 0,006 | <0,061 | 0,017 | 0,502 |
| 3 | 30,0 | 0,073 | 0,100 | 0,006 | 0,020 | 0,07 | 0,480 |
| 3 | 32,0 | 0,052 | 0,100 | 0,006 | 0,061 | 0,07 | 0,500 |
| 4 | 40,0 | <0,021 | <0,103 | 0,006 | 0,061 | 0,07 | 0,472 |
| 4 | 30,5 | 0,031 | 0,100 | 0,006 | 0,061 | 0,07 | 0,479 |
| 5 | 34,0 | 0,104 | <0,060 | 0,006 | 0,061 | 0,017 | 0,459 |
|
Примечания: 1. Сумма примесей дана с учетом других примесей, содержание которых во всех образцах составляло, ×10–4 %: <0,071 Cu; <0,038 Cr; 0,048 Zn; 0,017 Na; 0,037 V. 2. При подсчете суммы примесей принимали их максимальное значение, равное пределу чувствительности анализа, например <0,061 считали как 0,061. |
|||||||
Содержание примесей, в алюминии, дистиллированном через субфторид, находится в обратной зависимости от массы получаемых слитков. В слитках массой 1,5-1,7 кг суммарное содержание примесей (Si, Fe, Cu, Mg) составляет 11ּ10–4 %, а содержание газов 0,007 см3/100 г. Удельное остаточное сопротивление (ρ○) при температуре жидкого гелия для такого металла составляет (1,7÷2,0)ּ10–10 Омּсм. Дистилляция алюминия через субфторид имеет ряд недостатков (сравнительно небольшая производительность, недостаточно глубокая очистка от магния и др.), поэтому способ не получил промышленного развития.
Разработаны также способы получения алюминия особой чистоты электролизом комплексных алюминийорганических соединений, отличающиеся составом электролита. Например, в ФРГ применяют способ электролиза 50%-ного раствора NaFּ2Al (C2H5)3 в толуоле. Рафинирование проводят при 100°С, напряжении на электролизере 1,0-1,5 В и плотности тока 0,3-0,5 А/дм2 с использованием алюминиевых электродов. Катодный выход по току 99%. Электрохимическим рафинированием в алюминийорганических электролитах существенно снижается содержание марганца и скандия, которые практически не удаляются при зонной очистке. Недостатками указанного способа являются его низкая производительность и высокая пожароопасность.
Для более глубокой очистки алюминия и получения металла чистотой 99,99999% и более можно использовать комбинирование указанных выше способов: электролиз алюминийорганических соединений или возгонку через субфторид с последующей зонной плавкой полученного алюминия. Например, многократной зонной очисткой алюминия, полученного электролизом алюминийорганических соединений, удается получить металл особой чистоты с содержанием примесей, ×10–9 %: Fe 50; Si <500; Cu 10; Mg 30; Mn 5; Ti <500; Cr 20; Zn <50; Co <1; Ag <5; Sb <1 и Se 3.
Применение
Сочетание физических, механических и химических свойств алюминия определяет его широкое применение практически во всех областях техники, особенно в виде его сплавов с другими металлами. В электротехнике алюминий успешно заменяет медь, особенно в производстве массивных проводников, например, в воздушных линиях, высоковольтных кабелях, шинах распределительных устройств, трансформаторах (электрическая проводимость алюминия достигает 65,5% электрической проводимости меди, и он более чем в три раза легче меди; при поперечном сечении, обеспечивающем одну и ту же проводимость, масса проводов из алюминия вдвое меньше медных). Сверхчистый алюминий употребляют в производстве электрических конденсаторов и выпрямителей, действие которых основано на способности окисной пленки алюминия пропускать электрический ток только в одном направлении. Сверхчистый алюминий, очищенный зонной плавкой, применяется для синтеза полупроводниковых соединений типа AIII BV, применяемых для производства полупроводниковых приборов. Чистый алюминий используют в производстве разного рода зеркал отражателей. Алюминий высокой чистоты применяют для предохранения металлических поверхностей от действия атмосферной коррозии (плакирование, алюминиевая краска). Обладая относительно низким сечением поглощения нейтронов, алюминий применяется как конструкционный материал в ядерных реакторах.
В алюминиевых резервуарах большой емкости хранят и транспортируют жидкие газы (метан, кислород, водород и т. д.), азотную и уксусную кислоты, чистую воду, перекись водорода и пищевые масла. Алюминий широко применяют и оборудовании и аппаратах пищевой промышленности, для упаковки пищевых продуктов (в виде фольги), для производства разного рода бытовых изделии. Резко возросло потребление алюминия для отделки зданий, архитектурных, транспортных и спортивных сооружений.
В металлургии алюминий (помимо сплавов на его основе) — одна из самых распространённых легирующих добавок в сплавах на основе Cu, Mg, Ti, Ni, Zn и Fe. Применяют алюминий также для раскисления стали пред заливкой её в форму, а также в процессах получения некоторых металлов методом алюминотермии. На основе алюминия методом порошковой металлургии создан САП (спечённый алюминиевый порошок), обладающий при температурах выше 300°С большой жаропрочностью.
Алюминий используют в производстве взрывчатых веществ (аммонал, алюмотол). Широко применяют различные соединения алюминия.
Производство и потребление алюминия непрерывно растет, значительно опережая по темпам роста производство стали, меди, свинца, цинка.
2 DIN (Deutsch Industrienorm) — промышленный стандарт ФРГ.