
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
Психология и педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Рефераты по сексологии
Рефераты по информатике программированию
Краткое содержание произведений
Реферат: Коррозионные свойства титана и его сплавов
Реферат: Коррозионные свойства титана и его сплавов
Реферат по дисциплине: «Физические основы коррозии»
Выполнила ст. гр. ФМ - 505 Каримова Л. Р.
Уфимский государственный авиационный технический университет
Уфа - 2006 г
Введение
Создание новых технологий и производств приводит к применению агрессивных сред. Использование последних ставит вопрос о конструкционных материалах, стойких к их воздействию. Большой интерес в этом плане представляют металлы подгрупп титана и ванадия. Они уже нашли применение в современном приборостроении. Так, например, они широко используются в ракетной и авиационной технике, а также при создании ядерных реакторов.
Титан и титановые сплавы широко применяются в различных отраслях промышленности, благодаря высоким значениям удельной прочности и коррозионной стойкости.
Сплав ВТ6 относится к числу первых отечественных конструкционных титановых сплавов. В таблице 1 представлен химический состав сплава ВТ6.
Таблица 1 - Химический состав титанового сплава ВТ6.
|
Основные элементы |
Al | V | Примеси | Fe | Si | O | C | N | H | Zr |
| Содержание, % | 6,0 | 4,0 | Содержание не более, % | 0,3 | 0,1 | 0,2 | 0,1 | 0,05 | 0,015 | 0,3 |
Титан может участвовать во многих соединениях, он химически весьма активен. И в то же время титан является одним из немногих металлов с исключительно высокой коррозионной стойкостью: он практически вечен в атмосфере воздуха, в холодной и кипящей воде, весьма стоек в морской воде, в растворах многих солей, неорганических и органических кислотах. По своей коррозионной стойкости в морской воде он превосходит все металлы, за исключением благородных – золота, платины и т. п., большинство видов нержавеющей стали, никелевые, медные и другие сплавы. В воде, во многих агрессивных средах чистый титан не подвержен коррозии. Почему же это происходит? Почему так активно, а нередко и бурно, со взрывами, реагирующий почти со всеми элементами периодической системы титан стоек к коррозии?
Общие представление о коррозии металлов
Получение металлов из их природных соединений всегда сопровождается значительной затратой энергии. Исключение составляют только металлы, встречающиеся в природе в свободном виде: золото, серебро, платина, ртуть. Энергия, затраченная на получение металлов, накапливается в них как свободная энергия Гиббса и делает их химически активными веществами, переходящими в результате взаимодействия с окружающей средой в состояние положительно заряженных ионов:
Меn++
nе Ме0 (![]() G>0); Ме0 – ne Ме n+ (
G>0); Ме0 – ne Ме n+ (![]() G <0).
G <0).
металлургия коррозия
Самопроизвольно протекающий процесс разрушения металлов в результате взаимодействия с окружающей средой, происходящий с выделением энергии и рассеиванием вещества (рост энтропии), называется коррозией. Коррозионные процессы протекают необратимо в соответствии со вторым началом термодинамики.
Подсчитано, что около 20% ежегодной выплавки металлов расходуется в коррозионных процессах. Большой вред приносит коррозия в машиностроении, так как из-за коррозионного разрушения какой-нибудь одной детали может выйти из строя машина, стоящая нередко десятки и сотни тысяч рублей. Коррозия снижает точность показаний приборов и стабильность их работы во времени. Незначительная коррозия электрического контакта приводит к отказу при его включении. Меры борьбы с коррозионными процессами являются актуальной задачей современной техники.
Существенно влияет на коррозионные процессы уровень внешних или внутренних (остаточных) напряжений и их распределение в металле изделия.
Химической коррозии подвержены детали и узлы машин, работающих при высоких температурах, — двигатели поршневого и турбинного типа, ракетные двигатели и т. п. Химическое сродство большинства металлов к кислороду при высоких температурах почти неограниченно, так как оксиды всех технически важных металлов способны растворяться в металлах и уходить из равновесной системы:
![]() 2Ме(т) +
O2(г) 2МеО(т);
2Ме(т) +
O2(г) 2МеО(т);
![]() МеО(т) [МеО]
(р-р)
МеО(т) [МеО]
(р-р)
В этих условиях окисление всегда возможно, но наряду с растворением оксида появляется и оксидный слой на поверхности металла, который может тормозить процесс окисления.
Скорость окисления металла зависит от скорости собственно химической реакции и скорости диффузии окислителя через пленку, а поэтому защитное действие пленки тем выше, чем лучше ее сплошность и ниже диффузионная способность. Сплошность пленки, образующейся на поверхности металла, можно оценить по отношению объема образовавшегося оксида или другого какого-либо соединения к объему израсходованного на образование этого оксида металла (фактор Пиллинга—Бэдвордса).
Коэффициент (фактор Пиллинга — Бэдвордса) у разных металлов имеет разные значения и приведен в таблице 2.
Таблица 2. Значение коэффициента для некоторых металлов
| Металл | Оксид | | Металл | Оксид | |
| Mg | MgO | 0.79 | Zn | ZnO | 1.58 |
| Pb | PbO | 1.15 | Zr | ZrO2 | 1.60 |
| Cd | CdO | 1.27 | Be | BeO | 1.67 |
| Al | Al2O2 | 1.31 | Cu | Cu2O | 1.67 |
| Sn | SnO2 | 1.33 | Cu | CuO | 1.74 |
| Ni | NiO | 1.52 | Ti | Ti2O3 | 1.76 |
| Nb | NbO | 1.57 | Cr | Cr2O3 | 2.02 |
| Nb | Nb2O3 | 2.81 |
Металлы, у которых <1, не могут создавать сплошные оксидные слои, и через несплошности в слое (трещины) кислород свободно проникает к поверхности металла.
Сплошные и устойчивые оксидные слои образуются при = 1,2—1,6, но при больших значениях пленки получаются несплошные, легко отделяющиеся от поверхности металла (железная окалина) в результате возникающих внутренних напряжений.
Поведение титана и его сплавов в различных агрессивных средах
Реакции титана со многими элементами происходят только при высоких температурах. При обычных температурах химическая активность титана чрезвычайно мала и он практически не вступает в реакции. Связано это с тем, что на свежей поверхности чистого титана, как только она образуется, очень быстро появляется инертная, хорошо срастающаяся с металлом тончайшая (в несколько ангстрем (1А=10-10м) пленка диоксида титана, предохраняющая его от дальнейшего окисления. Если даже эту пленку снять, то в любой среде, содержащей кислород или другие сильные окислители (например, в азотной или хромовой кислоте), эта пленка появляется вновь, и металл, как говорят, ею «пассивируется», т. е. защищает сам себя от дальнейшего разрушения.
Рассмотрим несколько подробнее поведение чистого титана в различных агрессивных средах: в таких, как азотная, соляная, серная, «царская водка» и другие кислоты и щелочи.
В азотной кислоте, являющейся сильным окислителем, в котором быстро растворяются очень многие металлы, титан исключительно стоек. При любой концентрации азотной кислоты (от 10 до 99%-ной), при любых температурах скорость коррозии титана не превышает 0,1–0,2 мм/год. Опасна только красная дымящая азотная кислота, пересыщенная (20% и более) свободными диоксидами азота: в ней чистый титан бурно, со взрывом, реагирует. Однако стоит добавить в такую кислоту хотя бы немного воды (1–2% и более), как реакция заканчивается, и коррозия титана прекращается.
В соляной кислоте титан стоек лишь в разбавленных ее растворах. Например, в 0,5%-ной соляной кислоте даже при нагревании до 100° С скорость коррозии титана не превышает 0,01 мм/год, в 10%-ной при комнатной температуре скорость коррозии достигает 0,1 мм/год, а в 20%-ной при 20° С–0,58 мм/год. При нагревании скорость коррозии титана в соляной кислоте резко повышается. Так, даже в 1,5%-ной соляной кислоте при 100° С скорость коррозии титана составляет 4,4 мм/год, а в 20%-ной при нагревании до 60° С – уже 29,8 мм/год. Это объясняется тем, что соляная кислота, особенно при нагревании, растворяет пассивирующую пленку диоксида титана и начинается растворение металла. Однако скорость коррозии титана в соляной кислоте при всех условиях остается ниже, чем у нержавеющих сталей.
В серной кислоте слабой концентрации (до 0,5–1% ) титан и большинство его сплавов стойкие даже при температуре раствора до 50–95° С. Стоек титан и в более концентрированных растворах (10–20%-ных) при комнатной температуре, в этих условиях скорость коррозии титана не превышает 0,005–0,01 мм/год. Но с повышением температуры раствора титан в серной кислоте даже сравнительно слабой концентрации (10–20%-ной) начинает растворяться, причем скорость коррозии достигает 9–10 мм/год. Серная кислота, так же как и соляная, разрушает защитную пленку диоксида титана и повышает его растворимость. Ее можно резко понизить, если в растворы этих кислот добавлять определенное количество азотной, хромовой, марганцевой кислот, соединений хлора или других окислителей, которые быстро пассивируют поверхность титана защитной пленкой и прекращают его дальнейшее растворение. Вот почему титан практически единственный металл, не растворяющийся в «царской водке»: в ней при обычных температурах (10–20° С) коррозия титана не превышает 0,005 мм/год. Слабо корродирует титан и в кипящей «царской водке», а ведь в ней, как известно, многие металлы, и даже такие, как золото, растворяются почти мгновенно.
Очень слабо корродирует титан в большинстве органических кислот (уксусной, молочной, винной), в разбавленных щелочах, в растворах многих хлористых солей, в физиологическом растворе. А вот с расплавами хлоридов при температуре выше 375° С титан взаимодействует очень бурно.
В расплаве многих металлов чистый титан обнаруживает удивительную стойкость. В жидких горячих магнии, олове, галлии, ртути, литии, натрии, калии, в расплавленной сере титан практически не корродирует, и лишь при очень высоких температурах расплавов (выше 300–400° С) скорость его коррозии в них может достигать 1 мм/год. Однако есть немало агрессивных растворов и расплавов, в которых титан растворяется очень интенсивно.
Главный «враг» титана – плавиковая кислота (HF). Даже в 1%-ном ее растворе скорость коррозии титана очень высока, а в более концентрированных растворах титан «тает», как лед в горячей воде. Фтор – этот «разрушающий все» (греч.) элемент – бурно реагирует практически со всеми металлами и сжигает их.
Не может противостоять титан кремнефтористоводородной и фосфорной кислотам даже слабой концентрации, перекиси водорода, сухим хлору и брому, спиртам, в том числе спиртовой настойке йода, расплавленному цинку. Однако стойкость титана можно увеличить, если добавить различные окислители – так называемые ингибиторы, например, в растворы соляной и серной кислот – азотную и хромовую. Ингибиторами могут быть и ионы различных металлов в растворе: железо, медь и др.
В титан можно вводить некоторые металлы, повышающие его стойкость в десятки и сотни раз, например до 10% циркония, гафния, тантала, вольфрама. Введение в титан 20–30% молибдена делает, этот сплав настолько устойчивым к любым концентрациям соляной, серной и других кислот, что он может заменить даже золото в работе с этими кислотами. Наибольший эффект достигается благодаря добавкам в титан четырех металлов платиновой группы: платины, палладия, родия и рутения. Достаточно всего 0,2% этих металлов, чтобы снизить скорость коррозии титана в кипящих концентрированных соляной и серной кислотах в десятки раз. Следует отметить, что благородные платиноиды влияют лишь на стойкость титана, а если добавлять их, скажем, в железо, алюминий, магний, разрушение и коррозия этих конструкционных металлов не уменьшаются.
Влияние легирующих элементов в титане на коррозионную стойкость
Все присутствующие в титане легирующие элементы по коррозионной стойкости можно разделить на четыре группы.
К первой группе относятся легко пассивирующиеся элементы, повышающие коррозионную стойкость титана за счет торможения анодного процесса (в различной степени и в зависимости от природы среды). К этой группе относятся следующие наиболее важные легирующие: Мо, Та, Nb, Zr, V (расположены в порядке убывания благоприятного воздействия на коррозионную стойкость).
Ко второй группе металлов, оказывающих сходное влияние на коррозионную стойкость титана, относятся Cr, Ni, Mn, Fe. Эти элементы, некоторые из которых сами являются коррозионностойкими (Cr, Ni), хотя и не сильно, но снижают коррозионную стойкость титана, особенно в неокислительных кислотах по мере повышения легирования титана.
К третьей группе легирующих элементов, имеющих общие черты влияния на коррозионную стойкость титана, относятся Al, Sn, О, N, С. Установлено, что добавки алюминия снижают коррозионную стойкость титана в активном и пассивном состояниях. В нейтральных средах алюминий (до 5% Al) хотя и оказывает отрицательное влияние, но оно невелико. Понижение коррозионной стойкости при легировании алюминием связано с облегчением анодного и катодного процессов вследствие изменения химической природы пассивных пленок.
К четвертой группе легирующих элементов, однотипно влияющих на коррозионную стойкость титана, относятся металлы с низким сопротивлением катодному процессу. По возрастанию эффективности воздействия на титан эти элементы располагаются в следующий ряд: Си, W, Мо, Ni, Re, Ru, Pd, Pt.
Доказано, что введение в титановые сплавы таких элементов, как молибден, ниобий, цирконий, тантал не лимитируется по количеству. Они повышают коррозионную стойкость, способствуют увеличению прочности.
Электрохимическая коррозия под действием внутренних макро- и микрогальванических пар
Раньше электрохимическую коррозию называли гальванической коррозией, так как разрушение металла происходит под действием возникающих гальванических пар.
Рассмотрим различные случаи возникновения коррозионных гальванических пар.
1. Контакт с электролитом двух разных металлов в случае сочетания в одном узле или детали металлов различной активности в данной среде, или в случае применения сплава эвтектического типа из двух металлов разной активности.
2. Контакт металла и его соединения, обладающего металлообразными или полупроводниковыми свойствами. В любом случае свободный металл имеет отрицательный электрический заряд, а соединение — положительный заряд, так как в нем часть электронов проводимости связана. Это также справедливо и для интерметаллидов.
3. Различные концентрации электролитов или воздуха, растворенного в жидком электролите.
4. Различный уровень механических напряжений в одной и той же детали.
Рассмотрим более подробнее последний случай возникновения коррозионной гальванической пары. Коррозионные пары могут возникать при действии внешних или внутренних механических напряжений (остаточных напряжений, например при сварке). Если пластинку стали, дюраля или титанового сплава согнуть и в напряженном состоянии погрузить в коррозионную среду, то на растянутом слое (внешний) через относительно короткое время возникнут трещины (рис. 1), а внутренний сжатый слой будет оставаться без изменений. Растягивающие усилия особенно опасны, так как в этом случае металл повышает свою активность.
Рисунок 1 - Коррозия пластинки в напряженном состоянии
Если согнутую упруго пластинку (см. рис. 1) термически обработать и упругие деформации перейдут в пластические (явление релаксации), то разности потенциалов не возникает. Таким образом, при изготовлении деталей и узлов машин для снятия остаточных напряжений всегда следует термически обрабатывать изделия, если эти изделия предназначены для работы в сильно коррелирующих средах.
С этой целью в ИПСМ РАН при изготовлении тонких листов СМК - сплава ВТ6, полученных изотермической прокаткой, для более полного снятия остаточных напряжений и формирования зеренной структуры применяется крип-отжиг, который заключается в следующем: листы укладываются стопой между плоскими бойками и прижимаются под давлением 3-5 МПа при температуре 550 ˚С. После 20 мин выдержки нагрев выключается, и пакет остывает вместе со штамповым блоком в течение 12 часов.
Особенности взаимодействия титана с воздухом.
Воздух, представляющий собой смесь различных газов, является сложной газовой фазой, воздействие которой на титан может быть весьма многообразным. При этом взаимодействие титана с кислородом воздуха отличается от взаимодействия титана с чистым кислородом, так как на это взаимодействие оказывает влияние азот и другие составные части воздуха. Вместе с тем следует иметь в виду, что при всей сложности газовой фазы (воздуха) воздействие ее на титан следует рассматривать прежде всего как реакцию взаимодействия с ним самой активной и довольно значительной по количеству составляющей – кислорода.
Взаимодействие титана с кислородом.
При взаимодействии титана с кислородом происходит образование различных фаз химических соединений и твердых растворов.
При достаточно низких температурах взаимодействие титана с кислородом ограничивается адсорбцией. Начальная теплота адсорбции кислорода на титане при 25ОС составляет 989 кДж/моль; начальный коэффициент прилипания равен 1;0,8 и 0,67 при температурах -196; 25 и 300ОС соответственно. При дальнейшем взаимодействии на поверхности титана образуется оксидная плёнка.
В соответствии с термодинамическими расчетами оксидная пленка на титане должна состоять из слоев оксидов в последовательности:
Ti6O®Ti3O®Ti2O®Ti3O2®TiO®Ti13O5®TiO2
В действительности при окислении титана при температурах ниже 300OС оксидные слои состоят в основном из Ti3O5, при окислении в интервале температур 400-800OС образуется преимущественно рутил TiO2, а при температурах выше 800OС обнаружены оксиды TiO и Ti2O3. Согласно работе, окисление титана на воздухе и в кислороде до температур £ 600-650°С сопровождается образованием на образцах тонких оксидных пленок толщиной »0,1 мкм. Долей кислорода, растворенного в металлической основе при температурах ниже 450-500°С, по-видимому, можно пренебречь.
В работе [5] взаимодействие титана с кислородом описано следующим образом. Через возникающую на первых стадиях процесса пленку двуокиси титана TiO2 осуществляется диффузия кислорода к границе раздела пленка-металл, где происходит химическая реакция и дальнейший рост толщины пленки. Слой низших окислов титана, который должен присутствовать между слоем двуокиси и металлом, оказывается очень тонким и обычно не влияет на характер окисления. Скорость диффузии ионов титана через пленку по сравнению со скоростью диффузии титана очень мала. Однако при повышении температуры диффузия титана несколько увеличивается.
При небольшой продолжительности процесса, когда толщина пленки еще невелика, количество поступающего через пленку кислорода оказывается достаточным для окисления всего титана до двуокиси его. Вместе с тем по мере увеличения толщины пленки количество поступающего в зону кислорода уменьшается, а поступление титана остается постоянным, так как реакция происходит на границе раздела пленка-металл. В результате этого при достижении определенной толщины слоя окалины соотношение количеств титана и кислорода в зоне реакции становится таким, что между TiO2 и металлом образуется слой TiO. Появление его ослабляет сцепление окалины с металлом, которая под действием сжимающих напряжений деформируется и отслаивается, обнажая поверхность металла и обеспечивая скачкообразное увеличение скорости окисления. Однако возросшее поступление кислорода при отслаивании окалины приводит к окислению TiO до TiO2 и описанный выше процесс повторяется.
Газонасыщение титановых сплавов при окислении
Взаимодействие титана с кислородом сопровождается двумя параллельно идущими процессами: образованием оксидов и растворением кислорода в металлической основе.
При температурах ниже 8820С и нормальном давлении титан имеет гексагональную плотно упакованную решетку - a-Ti. Решетка a-Ti содержит четыре октаэдрических поры радиусом 0,414 rат.(0,60A) и восемь тетраэдрических пор радиусом 0,225 rат.(0,36A). Экспериментально установлено, что кислород, атомный радиус которого равен 0,60A растворяется в октапорах. Выше 8820С структура титана характеризуется объемноцентрированной решеткой - b-Ti. Решетка b-Ti содержит шесть октапор радиусом 0,115 rат.(0,22A) и двенадцать тетрапор радиусом 0,29rат.(0,41), то есть тетраэдрические пустоты в ОЦК-структуре более просторны. С позиций геометрии решеток a- и b-Ti растворение кислорода более благоприятно в высокотемпературной модификации.
В образовавшемся диффузионном слое выделяют альфированный и переходный слои. Альфированный слой отличается по структуре от основного металла повышенным содержанием a-фазы, что легко оценивается металлографическим анализом, часто этот слой представлен одной a-фазой. Переходный слой по микроструктуре не отличается заметно от основного металла, но его наличие и глубину проникновения можно оценить по более высокой микротвердости по сравнению с основным металлом.
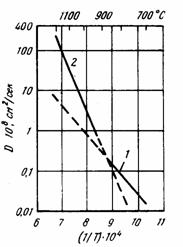
Рисунок 2-Зависимость коэффициентов диффузии кислорода от температуры:
в a-титане; 2- в b-титане.
Газонасыщение поверхности титанового сплава ВТ6.
В работе [6] проводилось исследование влияния газонасыщения на структуру и свойства титанового сплава ВТ6 на воздухе и в вакууме при температурах от 750 до 12000С и выдержках 5,30,60,180 и 360 минут.
Изменение микротвердости от поверхности вглубь образца в зависимости от температуры и времени выдержки представлено на рис 3. Микротвердость снижается от поверхности внутрь образца при всех режимах газонасыщения.
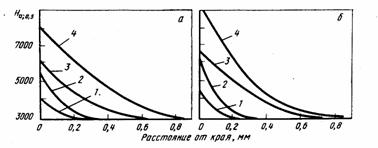
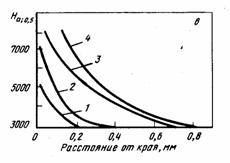
Рисунок 3 - Зависимость микротвердости титанового сплава ВТ6 от расстояния до поверхности после нагрева на воздухе в течение 1(а), 3(б) и 6(в)ч при 750(1), 950(2), 1050(3), 1200°С(4).
Нагрев сплава ВТ6 при сравнительно невысоких температурах 750-8000С в течение 1ч приводит к повышению поверхностной микротвердости от H300 до H400. Увеличение температуры и времени выдержки значительно интенсифицирует процесс газонасыщения вследствие увеличения скорости диффузии, в результате поверхностная микротвердость сильно повышается (рис.3). Так, увеличение времени выдержки от 1 до 6ч приводит при различных температурах к увеличению поверхностной микротвердости на H100-200.
При повышении температуры и увеличении времени выдержки увеличивается глубина газонасыщенного слоя (рис.4). Газонасыщенный слой формируется практически при выдержке в течение 1ч, а дальнейшее увеличение продолжительности газонасыщения мало влияет на глубину поверхностного газонасыщенного слоя.
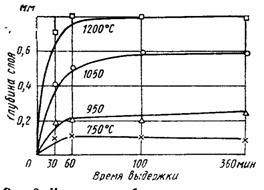
Рисунок 4 - Изменение глубины газонасыщенного слоя при различных температурах в зависимости от времени выдержки.
В работе [7] рассмотрены особенности газонасыщения титанового сплава ВТ6, которые заключаются в следующем. После выдержки при высокой температуре и последующего охлаждения на воздухе у сплава ВТ6 образуются трещины, которые выходят на поверхность. Причинами их возникновения являются внутренние напряжения и пониженная пластичность особо хрупкого газонасыщенного слоя. Фазовый состав и свойства поверхностного слоя резко отличаются от состава и свойств основного металла. В частности, температура полиморфного превращения этого слоя значительно выше, объемный эффект превращения меньше, а коэффициент линейного расширения больше, чем у основного металла. В результате при охлаждении внутренние части заготовки претерпевают меньшую температурную усадку и принудительно растягивают поверхностный слой. Возникающие при этом растягивающие напряжения в совокупности с пониженной пластичностью газонасыщенного слоя приводят к образованию трещин. При послойном измерении микротвердости после газонасыщенной зоны повышенной твердости идет небольшой участок, граничащий с основным металлом и имеющий по сравнению с ним пониженную твердость. Это объясняется процессами взаимной диффузии газов с поверхности вглубь металла и атомов основного металла и легирующих элементов к границе раздела газ-металл. В результате этого граница раздела металл - газонасыщенный слой оказывается обедненной легирующими элементами и дает пониженную твердость при испытании.
Явление коррозийного растрескивания
В металле, подверженном коррозионному растрескиванию, при отсутствии внешних напряжений обычно происходит очень незначительное коррозионное разрушение, а при отсутствии коррозионной среды под воздействием напряжений почти не происходит изменения прочности или пластичности металла. Таким образом, в процессе коррозионного растрескивания, т. е. при одновременном воздействии статических напряжений и коррозионной среды, наблюдается существенно большее ухудшение механических свойств металла, чем это имело бы место в результате раздельного, но аддитивного действия этих факторов. Коррозионное растрескивание является характерным случаем, когда взаимодействует химическая реакция и механические силы, что приводит к структурному разрушению. Такое разрушение носит хрупкий характер и возникает в обычных пластичных металлах, а также в медных, никелевых сплавах, нержавеющих сталях и др. в присутствии определенной коррозионной среды. При исследовании процесса хрупкого разрушения в результате коррозионного растрескивания особое значение имеет исследование раздельного воздействия на металл напряжений и коррозионной среды, а также их одновременное воздействие. Однако в процессе коррозионного растрескивания первостепенное значение имеют следующие стадии: 1) зарождение и возникновение трещин и 2) последующее развитие коррозионных трещин. Обе стадии, как будет показано ниже, являются индивидуальными ступенями в процессе коррозионного растрескивания.
Средами, в которых происходит коррозионное растрескивание металлов, являются такие среды, в которых процессы коррозии сильно локализованы обычно при отсутствии заметной общей поверхностной коррозии. Интенсивность локализованной коррозии может быть весьма значительной, в результате чего прогрессирует процесс развития очень узких углублений, достигая, вероятно, наибольшей величины на дне углублений, имеющих радиусы порядка одного междуатомного расстояния.
При воздействии на материал коррозионной среды, которая влияет на склонность сплава к коррозионному растрескиванию и характер разрушения, основными факторами являются следующие:
1) относительная разность потенциалов микроструктурных фаз, присутствующих в сплаве, что вызывает вероятность местного разрушения
2) поляризационные процессы на анодных и катодных участках
3) образование продуктов коррозии, которые оказывают влияние на коррозионный процесс.
Для того чтобы произошел процесс коррозионного растрескивания, необходимо наличие поверхностных или внутренних растягивающих напряжений. Обычно встречающиеся на практике разрушения обусловлены наличием остаточных напряжений, возникающих, при производстве и обработке металла, но в целях исследования не следует делать разграничения между остаточными напряжениями и напряжениями, возникшими в результате приложенных внешних нагрузок. Коррозионное растрескивание никогда не наблюдалось в результате действия поверхностных сжимающих напряжений; наоборот, сжимающие поверхностные напряжения разрушения могут использоваться для защиты от коррозионного растрескивания.
При увеличении величины приложенных напряжений уменьшается время до полного разрушения металла. Для коррозионного растрескивания обычно необходимы высокие напряжения, приближающиеся к пределу текучести, однако, часто разрушение может наступить и при напряжениях, значительно меньших предела текучести. Для многих систем сплавов наблюдается какой-то «порог» или «предел» напряжений, т. е. напряжения, ниже которых коррозионное растрескивание не происходит за определенный период времени. Такая зависимость, наблюдавшаяся, например, при замедленном растрескивании сталей, указывает, что основную роль в процессе разрушения играют напряжения.
Наиболее эффективный метод повышения устойчивости металлов против коррозионного растрескивания состоит в использовании соответствующих конструктивных мероприятий и способов обработки, сокращающих до минимума величину остаточных напряжений. Если остаточные напряжения неизбежны, успешно может быть применена термообработка, снимающая эти напряжения. Если позволяют условия, может быть использована, например, дробеструйная обработка, вызывающая сжимающие поверхностные напряжения, которые впоследствии дают возможность нагружать материал, не вызывая напряженного состояния поверхности. Одним из методов, который получает все большее признание и который связан с электрохимическим фактором процесса растрескивания, является применение катодной защиты.
Защита конструкций и машин, выполненных из титана и его сплавов, от коррозии
Защита конструкций выполненных из титана и его сплавов от коррозионного разрушения состоит из целого комплекса мероприятий по увеличению работоспособности и надежности данных конструкций и машин в коррозионной среде. Часть этих мер закладывается еще в процессе проектирования, часть — в процессе изготовления машин или конструкций, а остальные меры должны быть приняты в процессе эксплуатации.
1) Создание рациональных конструкций. Выбор материалов и их сочетаний для данного изделия, конечно, диктуется технической и экономической целесообразностью, но должен обеспечивать его коррозионную устойчивость. Конструктор должен предусмотреть рациональные формы частей машины, допускающие быструю очистку от грязи; машина не должна иметь мест скопления влаги, которая является возбудителем коррозии.
2)Обработка окружающей среды. Для разных видов коррозионных процессов обработка среды принимает различные формы. Сюда можно отнести удаление или снижение концентрации веществ, вызывающих или ускоряющих коррозионные процессы, а также введение замедлителей или ингибиторов коррозии.
Так, например, высокотемпературная газовая коррозия происходит главным образом за счет кислорода воздуха или других окисляющих сред, удалить кислород из которых нельзя, так как это нарушит работу машин (двигателей) или конструкций (оболочки, плоскости и т. д.). Поэтому обработка сводится только к удалению катализирующих веществ или веществ, наличие которых приводит к нарушению устойчивых оксидных слоев, пассивирующих металл.
На устойчивость оксидных слоев вредно влияет наличие галогенов, образующих летучие соединения. Поглощение галогенов или изменение состава окислительной среды (без галогенов) значительно повышает устойчивость металлических поверхностей.
К обработке среды можно в полной мере отнести и общие мероприятия по сохранению окружающей среды, требующие очистки промышленных и выхлопных газов, так как увеличение содержания в воздухе SO2, CO2, оксидов азота и других газов не только пагубно действует на окружающую природу, но и форсирует разрушение металлических конструкций в результате атмосферной коррозии, особенно в больших городах и вблизи промышленных предприятий.
В приборостроительной практике при герметизации схем обычно заменяют воздух на гелий или аргон высокой чистоты, что вообще исключает коррозию. Если есть возможность, то создается вакуум 1,33 • 10-2 — 1,33 • 10-3 Па. При необходимости сообщения приборного устройства с атмосферой и невозможности герметизации его ставят поглотители, сорбирующие влагу и диоксид углерода из воздуха и тем самым снижают возможность появления коррозионных пар.
3)Создание защитных покрытий. Цель их нанесения – предотвратить непосредственный контакт поверхности металлов, сплавов с агрессивными компонентами среды (Н2O, О2, Н+, NOx, SO2. SO3 и т.д.) Такие покрытия не только обеспечивают защиту от коррозии, но и сообщают изделиям эстетические качества (декоративность). Защитные покрытия должны быть более устойчивы к коррозии, чем защищаемые металлы. Такие покрытия должны быть сплошными, хорошо удерживаться на металлической основе (хорошая агдезия).